
分析 根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
解答 解:
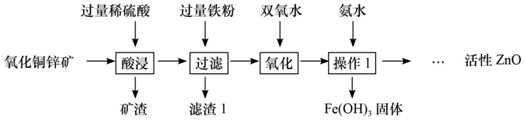
(1)操作1是得到难溶性氢氧化铁和硫酸锌溶液,所以是过滤.
(2)由于氧化铜锌矿主要成分为CuO和ZnO,在氧化铜锌矿中加入过量稀硫酸,氧化铜和硫酸反应生成硫酸铜,氧化锌和硫酸反应生成硫酸锌,所以充分反应后溶液中的溶质为生成的 ZnSO4和CuSO4以及剩余的H2SO4.
(3)由于是往酸浸过滤得到的溶液中加过量铁粉,该液体中有生成的 ZnSO4和CuSO4以及剩余的H2SO4.所以加入铁粉后,铁能够和硫酸铜反应生成硫酸亚铁和铜,铁和硫酸反应生成硫酸亚铁和氢气,对应的化学方程式为 Fe+CuSO4═FeSO4+Cu、Fe+H2SO4═FeSO4+H2↑.
(4)在实验过程中,双氧水会与Fe2+反应生成Fe3+和水,以便在后续的操作中将溶液中铁元素除去,而没有引入新的杂质.而高锰酸钾溶液也能将Fe2+氧化成Fe3+,并生成可溶性的锰盐,该可溶性锰盐对硫酸锌是新的杂质,所以选用双氧水的优点是最后的产物是水,不引入新的杂质.
故答案:
(1)过滤.
(2)ZnSO4、CuSO4、H2SO4.
(3)Fe+CuSO4═FeSO4+Cu、Fe+H2SO4═FeSO4+H2↑.
(4)最后的产物是水,不引入新的杂质.
点评 读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息扑捉的有效性.解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图提供的是情境,考查基本知识.


科目:初中化学 来源: 题型:实验探究题
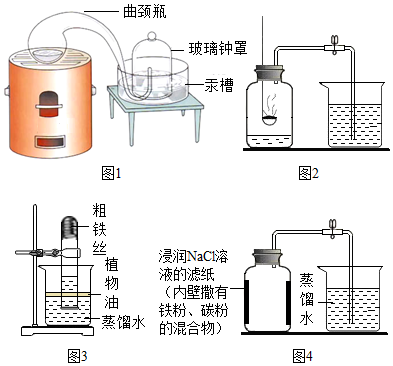
| 实验前的体积 | 实验后的体积 | |
| 集气瓶内空气 | 烧杯内蒸馏水 | 烧杯内剩余蒸馏水 |
| 131mL | 90.0mL | 63.6mL |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | BaCl2溶液 | 稀盐酸 | 加入过量碳酸钡、过滤 |
| B | KOH溶液 | KCl | 加入适量稀盐酸 |
| C | NaCl溶液 | Na2CO3 | 加入适量石灰水、过滤 |
| D | O2 | CO | 通过灼热的氧化铜 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
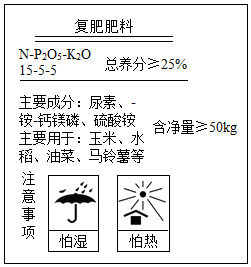 某复合肥的部分说明书如图所示,下列说法正确的是( )
某复合肥的部分说明书如图所示,下列说法正确的是( )| A. | 从肥效角度看,这种肥料共有两种营养元素 | |
| B. | 化肥能提高粮食产量,施用越多越好 | |
| C. | 从图示可知,这种复合肥料是可溶于水的 | |
| D. | 从图示可知,这种复合肥料受热不易变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
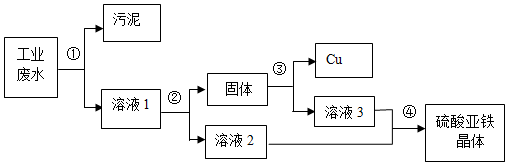
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 侯德榜制碱制得了烧碱 | |
| B. | 消石灰可用于改良酸性土壤 | |
| C. | 干冰、冰、可燃冰都属于氧化物 | |
| D. | 塑料、蛋白质、葡萄糖都属于高分子有机物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com