
请根据题22-1图回答相关问题:

A B C D
题22-1图
(1)仪器a的名称是 。
(2)A图称量前,要将天平调平衡,首先要把 ,然后才调节平衡螺丝;称量粉末状固体时若药品量不足,此时一只手用药匙取药品移至天平左盘上方,另一只手应 ,使少量药品落人盘中。
(3)上述图有明显错误的是 (填序号);c图中的玻棒作用是:搅拌,防止 。
 (4)D图的装置可用来制取的气体是 (写—种),制取该气体的化学方程式为:
(4)D图的装置可用来制取的气体是 (写—种),制取该气体的化学方程式为:
. ,该装置操作上的优点是 。
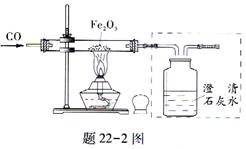
(5)题22-2图是利用CO还原Fe2O3的实验装置
图,玻璃管中固体的颜色变化是:. ;
集气瓶中的溶液用于检验和除去产生的CO2,
请把虚框中的图补充完整;处理尾气的方法是 。
【答案】(1)酒精灯 (2)游码归零 轻轻拍动拿钥匙的手
(3)B 受热不均液滴(或溶液)外溅
(4)O2(或CO2,或H2) 2H2O2MnO22H2O+O2↑(或CaCO3+2HCl=CaCl2+H2O+CO2↑,或Zn+H2SO4=ZnSO4+H2↑) 可控制滴入反应溶液的速度(或反应的速率,或快慢)
(5)由暗(或棕)红色变为黑色 (补画的图见右图) 点燃(或塑料袋收集)
【解析】(1)由图可知,仪器a是酒精灯;(2)调节天平平衡时,先将游码归零,再调节平衡螺丝;为防止加入药品过量,在添加药品时应轻轻拍动拿钥匙的手,使少量药品震落入盘中。(3)B中过滤时,漏斗下端管口应紧贴烧杯内壁;蒸发时需用玻璃棒搅拌,其目的是使液体受热均匀,防止液体外溅;(4)D图属于固液常温制取气体的发生装置,可用于制取氧气、二氧化碳、氢气等;用注射器代替长颈漏斗,便于控制滴加液体的速率,从而控制反应的快慢。(5)Fe2O3是红棕色固体,反应生成的铁粉是黑色固体,因此可观察到的现象是固体由红棕色变为黑色;为检验并吸收尾气中的CO2,应将气体通入溶液中,因此通入气体的导管要伸入液面下,导出尾气的导管少露出胶塞即可;尾气主要是CO,可用燃着的酒精灯点燃或者用气球、塑料袋等收集。


科目:初中化学 来源: 题型:
2013年12月1日起,汕尾市推广使用粤Ⅳ车用汽油。下列有关说法中正确的是( )。
A.汽油属于可再生能源
B.粤Ⅳ车用汽油是纯净物
C.粤Ⅳ车用汽油只含碳和氢两种元素
D.推广使用粤Ⅳ车用汽油有利于减少机动车尾气污染物的排放
查看答案和解析>>
科目:初中化学 来源: 题型:
用图2所示装置研究“活性炭吸附能力与温度变化的关系”。将NH4NO3固体加入到水中搅拌,观察到两侧玻璃管中液面上升的高度不同。
(1)由于试管内气体的压强 (选填“增大”或“减小”),使得玻璃管内液面上升。
(2)NH4NO3固体溶于水 (选填“放出”或“吸收”)热量。
(3)活性炭吸附气体的能力随温度 而增强。
查看答案和解析>>
科目:初中化学 来源: 题型:
重金属盐可使人中毒,当人误食重金属盐时,可以喝大量牛奶、鸡蛋清或豆浆解毒。原因是上述物质中含有较多的蛋白质,蛋白质可以和重金属盐形成不溶于水的化合物,可以减少重金属盐类对胃肠粘膜的危害,起到缓解毒性的作用,为了验证蛋白质与重金属盐类反应,形成难溶于水的化合物,我们可以做如下实验:
在一支试管中加入3 mL鸡蛋清溶液,再加少量的乙酸铅溶液,然后把试管中的物质倒入盛有清水的小烧杯中观察现象并回答问题:
(1)小烧杯中出现的现象
。
(2)为什么在农业上可以用硫酸铜配制的波尔多液来消灭害虫?
查看答案和解析>>
科目:初中化学 来源: 题型:
通过下列实验操作和现象能得出相应结论的是( )
| 实验操作 | 现象 | 结论 | |
| A | 向收集满CO2的软塑料瓶中加入约1/3体积的NaCl溶液,旋紧瓶盖,振荡 | 塑料瓶变瘪 | CO2能与NaCl反应 |
| B | 50℃时,将17gKCl固体加入50g蒸馏水中,完全溶解后缓慢降温 | 降温至20℃时开始有晶体析出 | 20℃时,KCl的溶解度为17g |
| C | 将白磷浸没在热水中,再向热水中的白磷通氧气 | 通氧气前白磷不燃烧,通氧气后白磷燃烧 | 氧气是燃烧需要的条件之一 |
| D | 点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁有无色液滴产生 | 该气体是CH4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
(1)用图I装置测定空气中氧气的含量,证明空气中氧气的体积分数约为1/5, a, b两
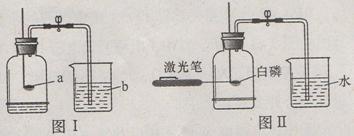 种物质可选用(填序号)。
种物质可选用(填序号)。
A.红磷、水
B.木炭、水
C.硫、NaOH溶液
D.小蜡烛、NaCl溶液
思敏同学对该实验进行反思后,提出了改进方法(如图II所示),你认为改进后的优点是(任写两点) 。
(2)“炭火烧烤”是许多同学喜爱的食物,其原理是利用木炭燃烧的高温来烤熟食物,炭燃烧反应的化学方程式是。冬天,在门窗紧闭的房间里吃“烧烤”,容易发生的危险是。如果在红热的木炭上撤一些氧化铁红棕色粉末,可能发生反应的化学方程式是 。
(3)冬季,园林工人在树干上涂石灰浆以保护树木免受虫害。某化学兴趣小组的同学
欲对工人用剩的石灰浆进行探究。
【提出猜想】石灰浆中除水之外的物质是什么?
I.只有Ca(OH)2; II.只有 ;III. 。
【实验验证】①要证明石灰浆中含有Ca(OH)2,可采取的操作及现象是。
②取石灰浆少量,盛装在试管中,如果向其中加入,观察到,则证明猜想II或III正确。
【思维拓展】工业上用石灰浆与Cl2反应制漂白粉,用来杀菌消毒。
① 配平下列化学方程式:Cl,+Ca(OH)=CaCl2+Ca(ClO)2+H,0
② 百度得知,漂白粉杀菌消毒的原理是:其中的Ca(CIO)2能与某些酸反应,生成的HCIO具有强氧化性,且不与CaCO3反应。写出CO2通人漂白粉溶液中发生反应的化学方程
式: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
为探究气体X的组成,某兴趣小组进行图所示实验(固定装置未画出)。
【资料在线】
(1)加热条件下,气体X能与氧化铜反应生成铜、水和氮气。
(2)碱 石灰为固体氢氧化钠和氧
石灰为固体氢氧化钠和氧 化钙的混合物,不与气体X反应。无水氯化钙可吸收气体X。
化钙的混合物,不与气体X反应。无水氯化钙可吸收气体X。
(3)本实验条件下,氮气密度为1.15g·L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计。
【实验步骤】
(1)连接仪器,并检查装置气密性。
(2)取一定量氧化铜,准确称得其质量为2.40g。
(3)按图所示装入药品,测量并记录相关数据Ⅰ(见表)。
(4)连接A、B、C装置, 将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热。当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却,再次测量并记录相关数据Ⅱ(见表)。
【实验装置】

【相关数据】
| 测量项目 数据编号 | I | II |
| 玻璃管(含药品)的质量/g | 52.40 | 51.92 |
| B装置(含药品)的质量/g | 102.00 | 102.54 |
| 氮气的体积/mL | 243.5 |
【回答问题】
⑴B装置中氧化钙吸水的原理为 (用化学方程式表示)。
⑵实验过程中,当观察到 ,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是 。
⑶分析 实验测量的数据,生成水的质量为 g,氧化铜中氧元素的质量为 g。由此推知,气体X中一定 (填“有”或 “没有”)氧元素。
实验测量的数据,生成水的质量为 g,氧化铜中氧元素的质量为 g。由此推知,气体X中一定 (填“有”或 “没有”)氧元素。
⑷通过计算推导出气体X的化学式。
查看答案和解析>>
科目:初中化学 来源: 题型:
氢氧化钙固体是登山运动员常用的能源提供剂。某探究小组的同学通过查阅资料得知,氢化钙(CaH2)遇水反应生成氢氧化钙和氢气。
探究小组的同学把一定量的CaH2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液。经检验滤渣的成分是碳酸钙。
【提出问题】滤液中溶质的成分是什么?
【猜想与暇设】猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、 Na2CO3 猜想四:NaOH、 Na2CO3、Ca(OH) 2
经过讨论,大家一致认为猜想四不台理,请用化学方程式说明原因_______________。
【实验验证】
| 实验 | 现象 | 结论 |
| 实验一:取滤液,向其中滴入少量碳酸钠溶液 | 无明显显现 | 猜想__不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 | ____________ | 猜想三成立 |
【反思与拓展】
①若向NH4Cl的溶液中加一定量的CaH2,充分反应,产生的气体是____________________。
②登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是_______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
我国劳动人民早在五千年前就会使用木炭炼铜。在化学实验室里模拟炼铜,既可用传统的实验装置(见图甲),又能用改进的微型实验装置(见图乙)。化学兴趣小组采用图乙装置,开展以下探究活动。

【提出问题】木炭与CuO反应所得红色固体中含有什么物质?
【查阅资料】(1)木炭与CuO的反应是:C + 2CuO  2Cu + CO2 ↑;若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O)。
2Cu + CO2 ↑;若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O)。
(2)Cu2O是红色固体,能与稀硫酸反应:Cu2O + H2SO4 = Cu + CuSO4 + H2O。
【作出猜想】红色固体的成分:①全部是Cu;②全部是Cu2O;③ ▲ 。
【实验探究】(1)取木炭、CuO两种黑色粉末适量,再与少许CaCl2(能降低反应温度、加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内。
(2)按图乙连好实验装置,然后加热反应物;2分钟后,黑色粉末出现红热现象,同时澄清的石灰水 ▲ ,此时停止加热。
(3)待玻璃管冷却后,提取里面的红色固体,进行如下的验证:
| 步 骤 | 现 象 | 结 论 |
| ①取1.44 g红色固体装入试管, 滴入足量的 ▲ ,充分反应 | 红色固体部分减少, 溶液变为 ▲ 色 | 猜想 ▲ 错误 |
| ②滤出试管中残留的红色固体, 洗涤干燥,称其质量为1.04 g | 猜想 ▲ 正确 |
【评价反思】(1)使用图乙装置与使用图甲装置相比,其优点是 ▲ (写出1条即可)。
(2)若要证明CaCl2是该反应的催化剂,还需要验证CaCl2的 ▲ 。
(3)在铜的冶炼史中,我国劳动人民还有一项重大发明就是“湿法炼铜”。该方法可用化学方程式表示为 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com