
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量反应后的溶液于试管中,逐滴加入碳酸钠溶液 | 只有白色沉淀产生 | 猜想(B)正确 |
| 先有气泡产生,后有白色沉淀产生 | 猜想(C)正确 |
分析 (1)根据题中的叙述找出反应物、生成物,根据方程式的书写规则进行书写方程式,氢氧化钙和盐酸反应生成了氯化钙和水;
【实验探究】
①根据酚酞遇碱变红来进行解答,根据碳酸盐会与酸反应生成二氧化碳气体进行分析;
②氯化钙溶液可以和碳酸钠溶液反应生成沉淀,和稀盐酸反应生成二氧化碳气体,所以可以据此解答,注意加入的碳酸钠溶液必须是足量的;
(3)根据酸会与铁反应进行分析,根据除杂的原则进行分析.
解答 解:(1)氢氧化钙和盐酸发生中和反应生成氯化钙和水,故答案为:Ca(OH)2+2HCl═CaCl2+2H2O;
①根据酚酞遇碱会变红色,而待测液体加入酚酞不变色,说明溶液不呈碱性,而猜想A的溶液呈碱性,所以可以排除;
②氯化钙溶液可以和碳酸钠溶液反应生成沉淀,和稀盐酸反应生成二氧化碳气体,碳酸钙盐酸存在的情况下不能以沉淀的形式析出,所以加入的碳酸钠溶液必须是足量的;
(3)盐酸会与铁反应而将下水道腐蚀;除去盐酸又不能引入新的杂质,还要防止过量,只能加碳酸钙;碳酸钙和盐酸反应生成氯化钙、水和二氧化碳.
故答案为:(1)Ca(OH)2+2HCl═CaCl2+2H2O;
【实验探究】
①酚酞溶液不变色,说明溶液不呈碱性,而猜想A的溶液呈碱性,所以可以排除.
②
| 实验步骤 | 预计现象 | 预计结论 |
| 取少量反应后的溶液于试管中,逐滴加入碳酸钠溶液. | 只有白色沉淀产生 | 猜想(B)正确 |
| 先有气泡产生,后有白色沉淀产生 | 猜想(C)正确 |
点评 解此类题时,首先对题中考查的问题进行全面的分析,然后再结合学过的知识进行解答,注意氯化钙中的盐酸只能用碳酸钙除去,根据溶解的情况,判断除杂的效果.


 天天练口算系列答案
天天练口算系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO具有还原性,可用于炼铁 | B. | CO2过多排放可导致酸雨的产生 | ||
| C. | CO易与血红蛋白结合引起中毒 | D. | CO2通入石蕊试液,溶液变红 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
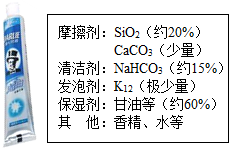 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题.
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题.| 实验编号 | 1 | 2 | 3 |
| 实验前(g) | 2.00 | 2.00 | 2.00 |
| 实验后(g) | 0.43 | 0.44 | 0.45 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com