
分析 (1)根据将溶液能使酚酞变红色分析;
(2)根据碱溶液能与二氧化碳反应;
(3)根据氢氧化钠溶液具有较强的腐蚀性解答;
(4)碳酸钠能与氢氧化钙反应生成碳酸钙沉淀分析.
解答 解:(1)无色酚酞溶液滴入NaOH、Ca(OH)2溶液中都会变成红色;
(2)NaOH、Ca(OH)2都能与空气中的二氧化碳反应生成碳酸钠、碳酸钙而变质;
(3)NaOH具有较强的腐蚀性,不能用来改良酸性土壤;
(4)碳酸钠能与氢氧化钙反应生成碳酸钙沉淀,而与氢氧化钠不反应,故可用碳酸钠来区分NaOH溶液和Ca(OH)2溶液;
答案:(1)红;(2)CO2;(3)腐蚀;
(4)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
点评 物质的组成和结构决定物质性质,本题难度不大,掌握酸与碱的化学性质是正确解答本题的关键.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:初中化学 来源: 题型:选择题
| A. | 原无色气体中可能只含有CH4和H2 | B. | 原无色气体中可能只含有CH4 | ||
| C. | 原无色气体中可能只含有CO和H2 | D. | 原无色气体中可能三种气体都有 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
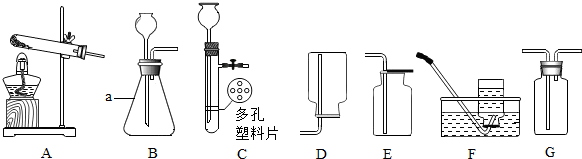
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 区分纯碱溶液和烧碱溶液:取样,分别滴入酚酞溶液,观察 | |
| B. | 检验一瓶无色气体是否为CO2:将燃着的木条伸入集气瓶中,观察 | |
| C. | 除去CuSO4溶液中的少量H2SO4:加入过量的Cu(OH)2,过滤 | |
| D. | 制取NaOH溶液:将饱和的石灰水与适量的氯化钠溶液混合,过滤 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气在低温、高压的条件下可以转化为液体或固体 | |
| B. | 氧气是植物光合作用的重要原料 | |
| C. | 氧气的化学性质比较活泼,是可燃物 | |
| D. | 氧气是可燃物燃烧的催化剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分离或制取物质与原理的对应关系 ①分离液态空气制取氧气、氮气等-物质沸点不同 ②可利用氯酸钾或高锰酸钾制取氧气的原因之一-物质中含有氧元素 | |
| B. | 燃烧事实与促进燃烧方法的对应关系 ①化油器将汽油喷成雾状,进入内燃机汽缸-增大可燃物与氧气的接触面积 ②用煤炭烧锅炉时,要用鼓风机不断吹入空气-增大氧气的浓度 | |
| C. | 化学概念与逻辑关系的对应 ①氧化反应与化合反应-交叉关系 ②单质与化合物-并列关系 | |
| D. | 物质性质与用途的对应关系 ①二氧化碳本身不燃烧也不支持燃烧-用于灭火 ②稀有气体几乎不与任何物质发生化学反应-用于制造霓虹灯 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
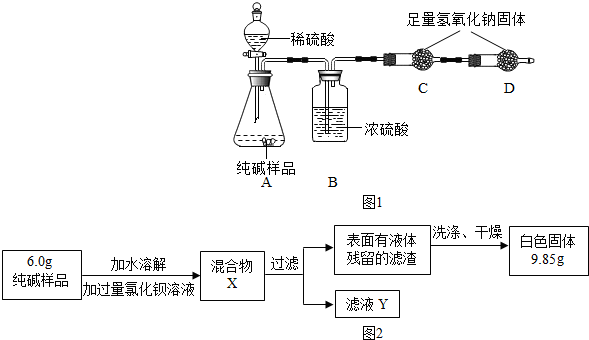
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com