

���� ��1����������ͭ�����ᷴӦ��������ͭ��ˮ���н��
��2�����ݷ�Ӧ�������������������������ͭ������������������ͭ�������������ͭ���������ɣ�
��3�����ŷ�Ӧ�Ľ��У���Ӧ����������٣������������������
��� �⣺��1����������ͭ�����ᷴӦ��������ͭ��ˮ������ʽΪCuO+H2SO4=CuSO4+H2O��
��2��������ͭ����ΪX��ͬʱ���������Ƶ�����ΪY��
CuSO4+2NaOH�TCu��OH��2��+Na2SO4
160 98 142
X 9.8g Y
$\frac{160}{X}$=$\frac{98}{9.8g}$
$\frac{98}{9.8g}$=$\frac{142}{Y}$
Y=14.2g
��3�����������������������ᷴӦ���������ƺ�ˮ����������ͭ��Ӧ����������ͭ�������ƣ������ڼ����������ƵĹ����У���������������������ʧ��Ȼ��������ͭ������������ʧ�����������������ӣ�
�ʴ�Ϊ����1��CuO+H2SO4=CuSO4+H2O�� ��2��$\frac{160}{X}$=$\frac{98}{9.8g}$
��3����������������������ʧ��Ȼ��������ͭ������������ʧ�����������������ӣ�
���� ������Ҫ����ѧ������ͼ��������Ϣ�Լ����û�ѧ����ʽ���м����������Ҫ���������������������Ӧ��ϵ����ȷ��д��ѧ����ʽ������˳�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���շϾɵ�� | B�� | ����ʹ�������Դ | ||
| C�� | ������ˮ���������ŷ� | D�� | ����ʹ��ũҩ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 200 | B�� | 150 | C�� | 73 | D�� | 173 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��1��������������������ͷ�չ����Ҫ���ʻ�����
��1��������������������ͷ�չ����Ҫ���ʻ������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�����̫���ܷ������ȼú���� | B�� | �ಿ����ץ���ܣ������ﳾ��Ⱦ | ||
| C�� | ��ũ����ո���ȼ�� | D�� | ����ʹ������Դ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
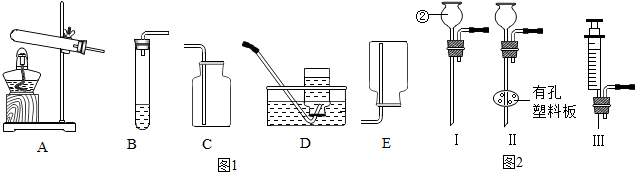
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
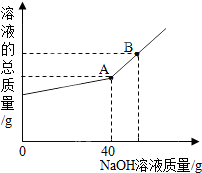 ��һ�ձ���ʢ��һ�������Ľ���þ�������м���������ϡ���ᣬ��ǡ����ȫ��Ӧ����һ���¶��µõ�30gMgSO4�IJ�������Һ����������Һ����ε���������������Ϊ10%��NaOH��Һ����Һ�������������NaOH��Һ��������ϵ������ͼ��ʾ�����������ش��������⣺
��һ�ձ���ʢ��һ�������Ľ���þ�������м���������ϡ���ᣬ��ǡ����ȫ��Ӧ����һ���¶��µõ�30gMgSO4�IJ�������Һ����������Һ����ε���������������Ϊ10%��NaOH��Һ����Һ�������������NaOH��Һ��������ϵ������ͼ��ʾ�����������ش��������⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com