
分析 根据物质的溶解度曲线可以判断随着温度的变化,物质的溶解度变化情况;
根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;
某温度下,饱和溶液的溶质质量分数最大,饱和溶液溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%;
根据物质的溶解度曲线、溶质质量、溶剂质量可以判断温度变化时是否析出晶体;
根据提供的数据可以进行相关方面的判断.
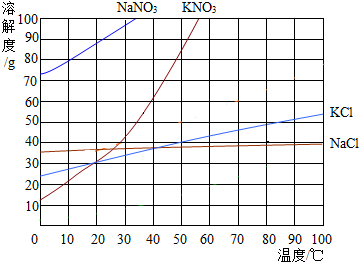
解答 解:(1)NaCl的溶解度随温度变化的规律是.
故填:随温度的升高而增大,但变化不大.
(2)20℃时KNO3和KCl的溶解度相等.
故填:20.
(3)50℃时,KCl的溶解度是40g,溶液的最大浓度为:$\frac{40g}{100g+40g}$×100%.
故填:$\frac{40g}{100g+40g}$×100%.
(4)20℃时,氯化钠的溶解度大于35g,硝酸钾的溶解度是30g,60℃时,氯化钠的溶解度大于35g,硝酸钾的溶解度大于90g,10gNaCl和90gKNO3完全溶解于100g蒸馏水,冷却到20℃后,没有NaCl析出,有60gKNO3结晶析出.
故填:没有;60.
(5)将该溶液恒温蒸发10g水后析出了1g晶体,变成了饱和溶液,再恒温蒸发5g水后,又析出了2g克晶体,说明5g水溶解2g溶质恰好饱和,因此1g溶质溶解在2.5g水中恰好饱和,如果保持温度不变,原溶液刚好达到饱和所需蒸发水的质量是10g-2.5g=7.5g.
故填:7.5.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
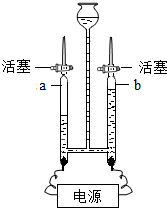 水是人类生活中不可缺少的物质.
水是人类生活中不可缺少的物质.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| V(O2)% | 实验现象 |
| 90% | 燃烧剧烈,燃烧时间长,实验成功 |
| 70% | 燃烧比90%的弱,燃烧时间短,实验成功 |
| 65% | 燃烧比70%的弱,燃烧时间比70%的短,实验成功 |
| 60% | 燃烧比65%的弱,燃烧时间更短,实验成功 |
| 55% | 难以燃烧,只是发红 |
| 实验操作 | 实验现象 |
取3根铁丝,将1根拉直,另两根绕成宽窄不同的螺旋状,进行如图所示实验. | 铁丝均燃烧,剧烈程度不同,II最剧烈,其次是 III,较弱的是 I. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水分子会停止运动 | B. | 水分子之间的间隔增大了 | ||
| C. | 水分子的体积增大了 | D. | 水分子体积和质量都很小 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
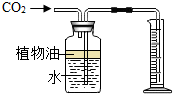 为研究实验室制取二氧化碳的速度与什么因素有关,科学兴趣小组的同学设计了如下实验方案:室温下在六个锥形瓶中分别加入A、B两种产地不同的大理石各50克,然后加入等量的不同溶质质量分数的稀盐酸.记录表如下:
为研究实验室制取二氧化碳的速度与什么因素有关,科学兴趣小组的同学设计了如下实验方案:室温下在六个锥形瓶中分别加入A、B两种产地不同的大理石各50克,然后加入等量的不同溶质质量分数的稀盐酸.记录表如下:| 试验次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 稀盐酸的溶质质量分数 | 5% | 10% | 15% | 5% | 10% | 15% |
| 大理石的种类 | A | A | A | B | B | B |
| 收集一瓶CO2所用的时间/秒 | 45 | 38 | 29 | 56 | 42 | 34 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 古代厅-徽派防火墙 | 近现代厅-灭火器 |
 |  |
| 防火防灾体验馆 | |
 |  |
| 常见的防火安全标志 | 火灾时,穿过浓烟 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 电解水的实验,说明化学变化中,分子可以再分 | |
| B. | 温度计中水银柱受热上升,说明温度升高,分子的间隔变大 | |
| C. | 原子得失电子可以变成离子,离子不能转化为原子 | |
| D. | 搜救犬能搜救地震中的幸存者,说明分子很小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com