
【题目】元素周期表是学习和研究化学的重要工具。如图是元素周期表的一部分,对相关信息表述正确的是( )
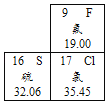
A. 氟原子的核内中子数为9
B. 氯原子的相对原子质量是35.45g
C. 氟、硫、氯三种元素都属于非金属元素
D. 氟元素和氯元素位于元素周期表的同一周期
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:初中化学 来源: 题型:
【题目】下图是实验室制取气体的常用仪器。请根据要求填空:
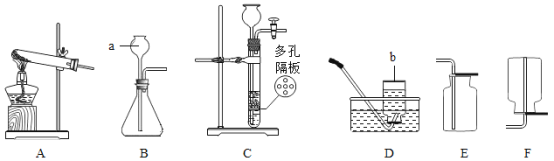
(1)写出图中仪器b的名称___________
(2)实验室用上图A装置(无棉花)来制取氧气,反应的化学方程式为________________,若用装置C来制备CO2,该装置的优点是___________
(3)已知氨气是一种无色有刺激性气味、极易溶于水、密度比空气小的气体。实验室常用加热氯化铵和熟石灰的固体混合物制取氨气,则其制取装置应选择______(填写装置的字母代号)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学方程式书写正确的是( )
A.4P+5O2![]() 2P2O5
2P2O5
B.CuO+CO═Cu+CO2
C.Zn+H2SO4═ZnSO4+H2
D.2KMnO4═K2MnO4+MnO2+O2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下图所示,调节杠杆平衡后开始进行实验。
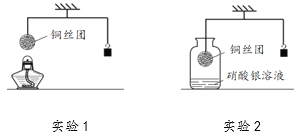
(1)实验1:加热细铜丝团一段时间后移走酒精灯,铜丝变为黑色(CuO),观察到细铜丝团________(填“上升”、“下降”或“不变”),出现上述现象的原因是________。
(2)实验2:将铜丝团浸入硝酸银溶液一段时间,当观察到溶液变为蓝色时小心地松手,发现稳定后的砝码比起始位置高,写出瓶中反应的化学方程式________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图所示。下列叙述正确的是( )
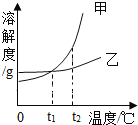
A. 当甲中含有少量乙杂质时,可以用将混合物在较高温度配制饱和溶液,冷却后析出甲晶体的办法得到纯甲晶体
B. 将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大
C. 将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温的方法
D. t1℃时,甲和乙的饱和溶液各100g,其溶质的质量不相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学要探究燃烧的条件和空气中氧气的含量,进行了如下实验.
【实验一】(已知:白磷的着火点为40℃)
实验装置 | 实验步骤及现象 |
| 步骤Ⅰ.检验装置的气密性,气密性良好. 步骤Ⅱ.将盛有白磷的带孔燃烧匙伸入A瓶中,白磷不燃烧. 步骤Ⅲ.向A瓶中加满80℃热水,塞紧瓶塞,白磷不燃烧. 步骤Ⅳ.打开K1、K2,从a口向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,关闭K1、K2.此时进入量筒B中水的体积为200mL,观察到A瓶中的白磷燃烧. |
(1)对比步骤Ⅱ和Ⅳ的现象可知,可燃物燃烧的条件之一是
(2)待装置冷却一段时间后,打开K2,如果观察到 ,说明空气中氧气的体积约占![]() .若实验测得空气中氧气的体积分数小于
.若实验测得空气中氧气的体积分数小于![]() ,原因可能是 (答一条即可).
,原因可能是 (答一条即可).
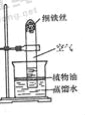
【实验二】用如图所示装置,利用铁生锈的原理也可以比较准确地测出空气中氧气的含量.若将此装置中的细铁丝换成足量的细铜丝进行实验,能否比较准确地测出空气中氧气的含量,并说明理由 .【已知:铜能与空气中氧气、水、二氧化碳反应生成铜绿.化学方程式:2Cu+O2+H2O+CO2═Cu(OH)2CO3】
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】随着经济的发展,能源与环境成为人们日益关注的问题.
(1)煤、_____、_____常称为化石燃料.
(2)燃煤发电时,将煤块粉碎成煤粉,其目的是_____.
(3)化石燃料燃烧都会产生二氧化碳,它是空气中含量最多的温室气体.为减少它的排放,科学家致力于研究将过多的二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷.该反应的化学方程式为_____.
(4)“绿色化学”的特点之一是“零排放”.一定条件下,二氧化碳和氢气可以按照不同比例反应,生成下列有机物.其中二氧化碳和氢气反应,只生成一种产物就能实现“零排放”,这种产物是_____(填字母序号).
A 甲醇CH4O B 甲酸CH2O2 C 乙醇C2H6O D 乙酸C2H4O2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】蔗糖(C12H22O11)是一种常用的食品甜味剂。下列关于蔗糖的说法正确的是( )
A. 蔗糖是由碳、氢、氧三种元素组成
B. 蔗糖中含有45个原子
C. 蔗糖中氢元素的质量分数最高
D. 蔗糖的相对分子质量为342g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。
(1)地壳中含量最高的金属元素是_____。
(2)根据下图的金属应用实例推断,金属具有的物理性质有_______

(3)日常使用的金属材料多数属于合金。下表列出了一些常见合金的主要成分和性能。
合金 | 合金的主要性能 | 主要成分及纯金属的性能 |
焊锡 | 熔点183℃ | 锡:熔点232℃;铅:熔点327℃。 |
硬铝 | 强度和硬度好 | 铝、铜、镁等。硬度小,质软。 |
不锈钢 | 抗腐蚀性好 | 铁、铬、镍等。纯铁抗锈蚀性能不如不锈钢。 |
由上表可以推断,与组成合金的纯金属相比,合金的优点一般有(填序号)______。
①强度更低 ②硬度更高 ③熔点更高 ④抗腐蚀性能更好
(4)2008年奥运会主运动场“鸟巢”使用了大量的钢铁。钢铁与_______、_______直接接触容易生锈造成损失,在钢铁表面涂油、刷漆等,都能防止钢铁生锈。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com