
分析 (1)根据质量守恒定律分析;
(2)化合物中,元素化合价的代数和为零;
(3)本题考查酸的概念,酸是由氢离子和酸根离子构成的.
解答 解:(1)根据质量守恒定律,反应前后原子的种类、数目都不变,反应前H的数目为4个,N的数目为4个,O的数目为12个;反应后H的数目为4个,N的数目为4个,O的数目为10个,所以X为O2;
(2)由于化合物中,元素化合价的代数和为零,设氮元素的化合价为y,所以(+1)+y+(-2)×4=0,解得y=+5;
(3)酸在电离的生成的阳离子全部是氢离子,所以具有一些共性.
故答案为:(1)O2;
(2)$\stackrel{+5}{{HNO}_{3}}$;
(3)H+
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
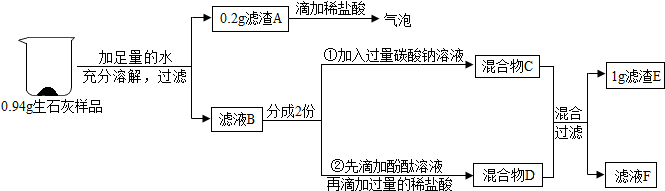
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 小倩同学的解法 | 小明同学的解法 |
| 解:设生成的铝质量为X 2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑ 204108 10t X $\frac{204}{108}$=$\frac{10t}{X}$ X=5.3t 答:最多可生产5.3t铝 | 解:氧化铝中铝元素的质量分数为 $\frac{Al的相对原子质量}{A{l}_{2}{O}_{2}的相对分子质量}$×100% $\frac{27×2}{27×2+16×3}$×100%=53% 铝的质量为10t×53%=5.3t 答:最多可生产5.3t铝 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
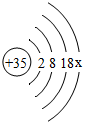 ,该元素符号为Br.图中x=7,Br属于非金属元素(填金属或非金属).下图表示的微粒中,具有相对稳定结构的是C(填序号,下同),与Br化学性质相似的是E.
,该元素符号为Br.图中x=7,Br属于非金属元素(填金属或非金属).下图表示的微粒中,具有相对稳定结构的是C(填序号,下同),与Br化学性质相似的是E.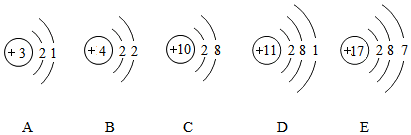
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
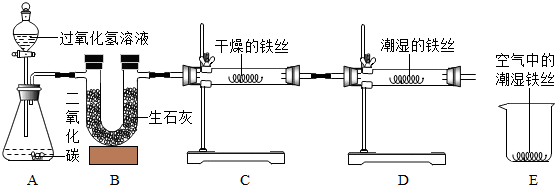
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验 装置 | 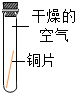 | 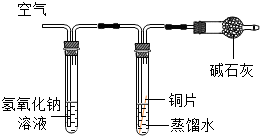 | 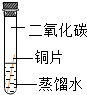 | 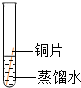 |
| 实验 现象 | 铜片不生锈 | 铜片不生锈 | 铜片不生锈 | 铜片生锈且水面 附近锈蚀最严重 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原子在不停运动 | B. | 分子在不停运动 | C. | 分子的质量很小 | D. | 分子之间有间隔 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com