【答案】
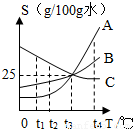
分析:由溶解度曲线,可以判断该温度下25gA、B、C三种固体分别加入100g水中中的溶解情况;t
1℃时C的溶解度为大于25g,可以判断其溶质的质量分数大小;t
1℃时,三种物质的溶解度大小,可以确定三种溶液的溶质质量分数的大小;由(3)可知,在t
1℃时,三种物质的饱和溶液中溶质的质量分数:C>B>A;由于A和B的溶解度随温度的升高而增大,t
4℃时AB的溶解度均大于25g,因此升温至t
4℃时,A和B的溶液中的剩余晶体会继续溶解且全部溶解,故在t
4℃℃时三种物质的溶解度B=A,而由于C的溶解度随温度的升高而减小,因此升温至t
4℃时,它的不饱和溶液就会变成饱和溶液,C的溶液中溶质的质量分数减小,故可以判断t
4℃,三种溶液的溶质质量分数的大小.
解答:解:A、t
1℃时,C的溶解度大于25g,AB的溶解度均小于25g,故将25gA、B、C三种固体分别加入100g水中,AB形成的是饱和溶液,C形成的是不饱和溶液;
B、t
1℃时C的溶解度为大于25g,故溶液的溶质质量分数大于
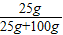
×=20%,故B说法错误;
C、t
1℃时,三种物质的溶解度大小是C>B>A,将25gA、B、C三种固体分别加入100g水中,溶液的溶质的质量分数的大小是C>B>A;
D、由(3)可知,在t
1℃时,三种物质的饱和溶液中溶质的质量分数:C>B>A;由于A和B的溶解度随温度的升高而增大,t
4℃时AB的溶解度均大于25g,因此升温至t
4℃时,A和B的溶液中的剩余晶体会继续溶解且全部溶解,故在t
4℃℃时三种物质的溶解度B=A,而由于C的溶解度随温度的升高而减小,因此升温至t
4℃时,它的不饱和溶液就会变成饱和溶液,C的溶液中溶质的质量分数减小,故t
4℃,三种溶液的溶质质量分数的大小关系为A=B>C.
故选BD.
点评:本题难度不大,主要考查了固体溶解度曲线所表示的意义,通过本题可以加强学生对固体溶解度的理解,培养学生应用知识解决问题的能力.

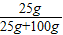 ×=20%,故B说法错误;
×=20%,故B说法错误;

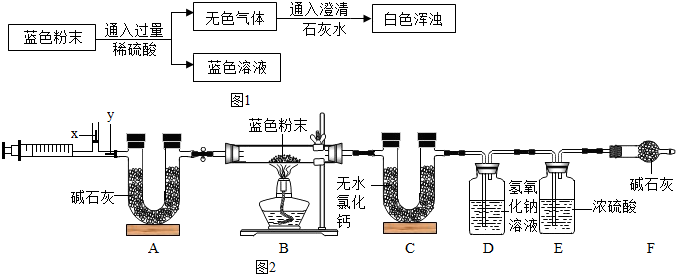
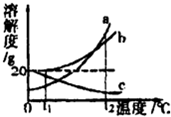
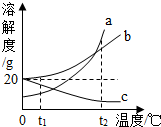 (2012?香坊区一模)a、b、c三种物质的溶解度曲线如图所示.tl℃时取a、b、c三种物质各20g分别加入到100水中,充分溶解后,得到三种混合物.下列说法正确的是( )
(2012?香坊区一模)a、b、c三种物质的溶解度曲线如图所示.tl℃时取a、b、c三种物质各20g分别加入到100水中,充分溶解后,得到三种混合物.下列说法正确的是( )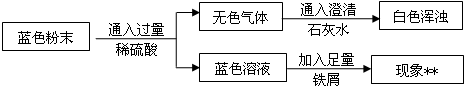
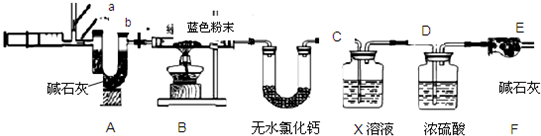
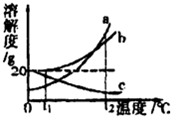 a、b、c三种物质的溶解度曲线如图所示.tl℃时取a、b、c三种物质各20g分别加入到100水中,充分溶解后,得到三种混合物.下列说法正确的是
a、b、c三种物质的溶解度曲线如图所示.tl℃时取a、b、c三种物质各20g分别加入到100水中,充分溶解后,得到三种混合物.下列说法正确的是