
| 物质 | X | Y | Z | Q |
| 反应前的质量(g) | 1 | 2 | 15 | 15 |
| 反应后的质量(g) | 16 | a | 5 | 10 |
| A. | 该反应属于化合反应 | B. | 反应后X和Y的质量之比为8:1 | ||
| C. | Q和Z的相对分子质量之比为1:2 | D. | Y可能不是该反应的催化剂 |
分析 由题意可知,根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,则可求“未测”值;反应后质量增加的物质是生成物,反应后质量减小的物质是反应物,反应前后质量没有变化的物质可能是催化剂,也可能既不是反应物,也不是生成物,结合图中数据进行分析即可.
解答 解:由题意可知,根据质量守恒定律,反应前各物质的质量总和=反应后生成各物质的质量总和,设未测值为a,则可列式:1+2+15+15=16+a+5+10,解得a=2;
反应后:X的质量增加了16g-1g=15g,X是生成物;Y的质量不变,可能是该反应的催化剂,也有可能没有参与反应;Z的质量减少了15g-5g=10g,属于反应物;Q的质量减少了15g-10g=5g,属于反应物.
A.该反应是由Z+Q→X,属于化合反应,故正确;
B.反应后X和Y的质量之比为:16g:2g=8:1,故正确;
C.反应中Q与Z的质量比为:5g:10g=1:2,因为不知道Q、Z前的化学计量数,所以无法确定二者的相对分子质量比,故错误;
D.物质Y的质量在反应前后不变,可能是该反应的催化剂,也可能没有参与化学反应,故正确.
故选C.
点评 根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:初中化学 来源: 题型:选择题
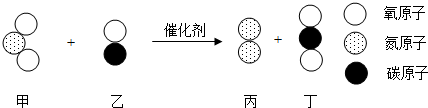
| A. | 变化前后氮原子和氧原子的个数均发生改变 | |
| B. | 甲、乙、丁三种物质均属于氧化物 | |
| C. | 乙和丁两种物质的组成元素相同,所以它们的化学性质相同 | |
| D. | 此反应的基本反应类型为置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CH4+O2$\stackrel{点燃}{→}$CO2+2H2O | B. | 2KMnO4$\stackrel{△}{→}$K2MnO4+MnO2+O2↑ | ||
| C. | CaCO3+H2O+CO2→Ca(HCO3)2 | D. | CuSO4+2NaOH→Cu(OH)2↓+Na2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| A的质量 | B的质量 | 得到AB的质量 | |
| 甲 | 7g | 2g | 6g |
| 乙 | 4g | 5g | 6g |
| 丙 | 5g | 4g | 7.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
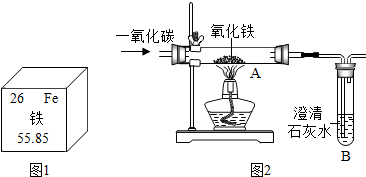

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
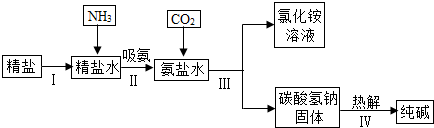
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲醛对人体健康有害 | |
| B. | 纳米TiO2与普通的TiO2的性质、功能完全相同 | |
| C. | 纳米TiO2添加到墙面涂料中,可降低甲醛污染 | |
| D. | 制备纳米TiO2的反应:H4TiO4$\frac{\underline{\;一定条件\;}}{\;}$Ti02+2H20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com