
【题目】写出下列化学反应方程式
(1)高温煅烧石灰石_____。
(2)稀硫酸与铁锈反应_____。
(3)铜和硝酸银溶液_____。
(4)硫酸铵和氢氧化钠溶液混合共热_____。
(5)小苏打中加入稀盐酸_____。
【答案】CaCO3![]() CaO+CO2↑ Fe2O3+3H2SO4═Fe2(SO4)3+3H2O Cu+2AgNO3=2Ag+Cu(NO3)2 (NH4)2SO4+2NaOH
CaO+CO2↑ Fe2O3+3H2SO4═Fe2(SO4)3+3H2O Cu+2AgNO3=2Ag+Cu(NO3)2 (NH4)2SO4+2NaOH![]() Na2SO4+2H2O+2NH3↑ NaHCO3+HCl=NaCl+H2O+CO2↑
Na2SO4+2H2O+2NH3↑ NaHCO3+HCl=NaCl+H2O+CO2↑
【解析】
首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可。
(1)石灰石的主要成分是碳酸钙,在高温的条件下,碳酸钙分解为氧化钙和二氧化碳;故填:CaCO3![]() CaO+CO2↑
CaO+CO2↑
(2)铁锈的主要成分是氧化铁,氧化铁能与稀硫酸反应生成硫酸铁和水,故填:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
(3)铜与硝酸银反应生成银和硝酸铜;故填:Cu+2AgNO3=2Ag+Cu(NO3)2
(4)硫酸铵与氢氧化钠反应生成硫酸钠、水和氨气;故填:(NH4)2SO4+2NaOH![]() Na2SO4+2H2O+2NH3↑
Na2SO4+2H2O+2NH3↑
(5)小苏打是碳酸氢钠的俗称,碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳;故填:NaHCO3+HCl=NaCl+H2O+CO2↑


科目:初中化学 来源: 题型:
【题目】有A~F六种物质,已知A、B、C三种固体含有同种金属元素,A是大理石、石灰石的主要成分,B是一种氧化物能与E反应放出大量的热,D、E、F含有同种非金属元素,E通常状况下为液体,D、F通常状况下为气体,且F为单质。它们的转化关系如图(部分产物已略去)。温馨提示:图中“→”表示箭尾的物质可转化成箭头的物质;“﹣”表示两端的物质能发生化学反应。
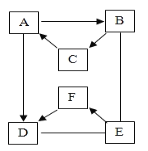
(1)写出A、E物质的名称:A_____,E_____。
(2)写出C→A的化学方程式:_____。
(3)写出E→F的化学方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】没有水就没有地球上的生命,人类的日常生活离不开水。
(1)日常生活中常用的净化水的操作有沉淀、过滤、吸附、蒸馏等,其中能把硬水软化的操作是_________。
(2)写出电解水的化学反应方程式:___________;该反应的基本类型是_____。
(3)A、B、C三种固体的溶解度曲线如图所示:①P点的含义是______________;②t1℃时,将10gA物质加入50g水中,充分溶解后,形成溶液的质量为____ g;
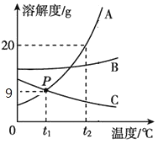
③t2℃时,将A、B、C物质饱和溶液各100克,分别蒸发10克水后,剩余溶液质量分数由大到小的顺序是________。
(4)氢氧化钠是实验室中常见的碱,现用氢氧化钠固体配制溶质质量分数为40%(密度为1.43g/mL)氢氧化钠溶液100mL,过程如下:
①计算:需称量氧氢化钠固体__________ g,加水体积为___________mL。
②称量:如图称量氢氧化钠固体的操作中,有一处明显错误是________________________。
③溶解:将正确操作称量好的氢氧化钠固体加入烧杯中,并将量取的蒸馏水倒入烧杯中,并用玻璃棒搅拌,使它完全溶解。经检测,所配制溶液的溶质质量分数偏小,其原因可能是_________(填序号)。

①氢氧化钠固体不纯 ②量取水时,俯视读数
③量取水时,仰视读数 ④装瓶时,有少量溶液洒出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学基础与常识
(1)下图金属应用的实例,主要利用金属的导热性的是_______(填序号);

A电缆 B.电热壶 C.金属丝 D.金属乐器
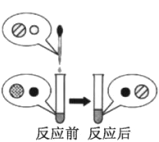
(2)向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“○”“![]() ”“●”“
”“●”“ ![]() ”表示不同离子)。则“○”与“
”表示不同离子)。则“○”与“![]() ”反应生成了_________(填物质名称)。
”反应生成了_________(填物质名称)。
(3)氢氟酸(HF)能刻画玻璃,其中有一个化学反应的化学方程式是:CaSiO3+6HF=X+SiF4↑+3H2O,则X的化学式为_______________
(4)氢能是一种极具发展潜力的清洁能。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示。
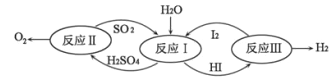
写出反应I中,发生反应的化学方程式:_____________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图所示的四个实验,得出的结论正确的是( )
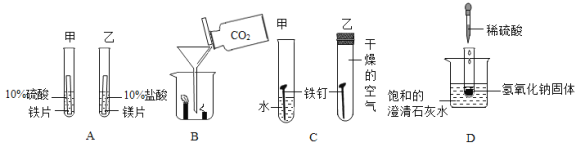
A. 乙试管中产生气泡速率大于甲试管中产生气泡速率,说明金属活动性:镁>铁
B. 蜡烛由低到高依次熄灭,说明通常状况下CO2不能燃烧,不支持燃烧,密度大于空气
C. 甲试管中的铁钉生锈,乙试管中的铁钉不生锈,说明只需与水接触铁钉就会生锈
D. 向盛有NaOH固体的试管中滴加稀硫酸,烧杯中饱和的澄清石灰水变浑浊,说明H2SO4与NaOH发生中和反应放出热量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】大黄同学喝“养乐多”时感觉有酸味,他猜测其中有酸。査阅资料大黄同学得知,养乐多含有乳酸。
(提出问题)乳酸是否具有酸的通性?
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
在乳酸溶液中加入石蕊 | 石蕊变红 | 乳酸具有酸的通性 |
在乳酸溶液中加入_____(填化学式) | 有气泡产生,点燃气泡产生爆鸣声 | |
在乳酸溶液中加入碳酸氢钠 | _____ |
(实验反思)(1)从微粒角度看,乳酸具有酸的通性是因为其溶液中存在大量_____;
(2)乳酸化学符号用HL表示,写出乳酸和碳酸氢钠反应的化学方程式_____。
(定量研究)为测定乳酸组成元素和化学式,称取6.0g乳酸放入如图加热装置中(夹持仪器未画出),通入充足氧气使之完全燃烧,将反应后的混合气体先后通过装置B、C.试回答:

(1)为顺利完成实验,将方框内所示装置放入B、C位置时,正确的导管连接顺序是:_____→_____→_____→_____;
(2)按正确方式连接B、C装置进行实验,实验后测得氢氧化钠溶液增重_____g,浓硫酸增重3.6g,则乳酸中碳元素:氢元素质量比=6:1;
(3)已知乳酸相对分子质量是90,则乳酸的化学式为_____。
(反思拓展)乳酸经过聚合反应可以制成聚乳酸塑料[(C3H4O2)n,n>1000],聚乳酸塑料常温下会降解生成CO2和H2O.以下对聚乳酸认识正确的是_____。
A 聚乳酸制成的外卖快餐饭盒,不会产生“白色污染”
B 聚乳酸是一种有机高分子化合物
C 聚乳酸降解发生了分解反应
D聚乳酸中碳元素:氢元素:氧元素质量比=9:1:8
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】被国外友人称作“新四大发明之一”的高铁,大大方便人们的出行。

(1)图中标示的物质中为金属材料的是______(填序号),动车电路中的导线大多选用铜制造的,这是利用了铜的延展性和__________性。
(2)动车表面喷漆主要是为了防止外壳生锈,其原理是________。
(3)修建铁路所需的大量钢铁是以铁矿石为主要原料冶炼而得。写出一氧化碳和赤铁矿炼铁的化学方程式:_______________。
(4)已知M、N、R三种金属存在如下反应:R+NCl2=== N+RCl2;M+RCl2===R+MCl2,M、N、R三种金属的活动性由强到弱的顺序为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素周期表是我们学习和研究化学的重要工具.下表是元素周期表1号~18号元素原子核外电子排布,我对它进行研究:
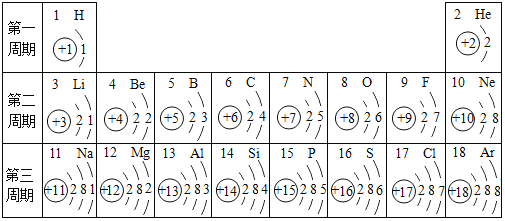
(1)第13号元素属于________元素(填“金属”或“非金属”),它在化学反应中容易________(填“得”或“失”)电子,它的离子符号为________。
(2)从上表中我还可以探究出以下规律:原子核外电子数等于原子序数、等于______、等于______。
(3)研究表明:第二周期从3号--9号元素的原子电子层数相同,核电荷数逐渐增大,核对核电子的引力逐渐增大,故原子半径逐渐减小.我分析第三周期从11号--17号元素原子半径变化规律是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com