
科目:初中化学 来源: 题型:
| A、0.9g | B、2.25g |
| C、7.5g | D、9g |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
| A、10℃时,将40 g NaCl固体加入100 g水中,可得到140 g NaCl溶液 |
| B、KNO3和NaCl的溶解度受温度的影响都很大 |
| C、将30℃的KNO3饱和溶液升温至60℃,会变成不饱和溶液 |
| D、20℃时,NaCl饱和溶液的溶质质量分数为36% |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、洗涤剂去油污是因为乳化作用 |
| B、节约水资源就是提高水的利用效益 |
| C、电脑一旦失火应立即用水浇灭 |
| D、湿衣服晾干是因为分子不断运动 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、溶液一定是无色透明的液体 |
| B、不饱和溶液降低温度后一定变成饱和溶液 |
| C、浓溶液可能是不饱和溶液 |
| D、溶质可以是固体、气体或液体 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

| 阴离子 阳离子 | OH- | NO3- | Cl- | SO42- | CO32- |
| H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 溶 | 不溶 | 不溶 |
| 实验目的 | 实验操作 | 现象 | 结论或化学方程式 |
除去碳酸钠 | 取少量该固体样品溶于水配成溶液,滴加适量的 充分反应后过滤 | 有白色沉淀生成 | 有关反应的化学方程式为 |
| 检验是否含有氢氧化钠 | 在滤液中滴加酚酞溶液 | 该样品中含有氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 序号 | 样品 | 量筒起始 读数/mL | 量筒最终 读数/mL | 所需时间 /min |
| ① | 1g铁粉、0.2g碳和10滴水 | 100 | 78 | 约120 |
| ② | lg铁粉、0.2g碳、10滴水和少量NaCl | 100 | 78 | 约70 |
| ③ |  |  |  |
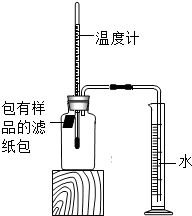 (1)实验①和②说明NaCl可以
(1)实验①和②说明NaCl可以查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com