

分析 【实验和推断】(1)根据碳酸钠和盐酸反应会生成氯化钠、水和二氧化碳进行分析;
(2)根据氢氧化钙和碳酸钠反应会生成碳酸钙沉淀和氢氧化钠,引入了氢氧根离子进行分析;
(3)根据氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠进行分析;
【反思】根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析.
解答 解:【实验和推断】(1)碳酸钠和盐酸反应会生成氯化钠、水和二氧化碳,所以若现象a为有气泡产生,则加入的A溶液是稀盐酸,说明氢氧化钠已经变质,有气泡产生的反应的化学方程式是:Na2CO3+2HCl=2NaCl+CO2↑+H2O,该反应的基本反应类型为复分解反应;
(2)氢氧化钙和碳酸钠反应会生成碳酸钙沉淀和氢氧化钠,引入了氢氧根离子,所以若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则白色沉淀为CaCO3,该实验不能说明样品中有NaOH;
(3)氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,所以若A是CaCl2溶液,当实验现象a为有白色沉淀产生,现象b为无色酚酞试液不变红色,则猜想Ⅱ成立;
【反思】根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析.
故答案为:【实验和推断】(1)稀盐酸,Na2CO3+2HCl=2NaCl+CO2↑+H2O,复分解反应;
(2)CaCO3,不能;
(3)有白色沉淀产生,无色酚酞试液不变红色;
【反思】2NaOH+CO2═Na2CO3+H2O.
点评 本考点考查了氢氧化钠在空气中的变质情况,还考查了化学方程式的书写.实验探究题包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 Q盐溶液能给酸X、碱Y、盐Z进行如图所示的反应.请推断并写出符合要求的三个化学反应的方程式.
Q盐溶液能给酸X、碱Y、盐Z进行如图所示的反应.请推断并写出符合要求的三个化学反应的方程式.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 4.4 | 12.8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
| A. | 表中a的值为5.6 | B. | X中含有碳元素 | C. | X中含有氧元素 | D. | X中含有氢元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
实验步骤 | 实验现象 | 结论 |
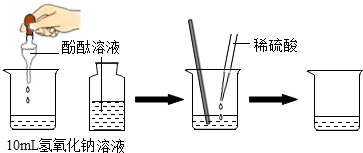
①向烧杯中加入10mL氢氧化钠 溶液,并滴入几滴酚酞溶液; ②再用滴管慢慢滴入稀硫酸,并不断搅拌溶液 | ①溶液颜色变红; ②不断搅拌溶液至溶液颜色恰好变成无色为止 | 酸和碱发生了中和反应,该反应属四种基本反应类型中的复分解反应 |
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 硫酸过量 |
方案二 | 取样,滴入几滴无色酚酞溶液 | 酚酞溶液不变色 | 酸、碱恰好反应 |
方案三 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 硫酸过量 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
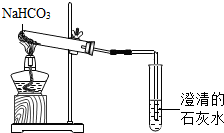 碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小刚用如图所示装置进行实验:取少量碳酸氢钠粉末,充分加热后,观察到大试管口有水珠出现,管底有白色固体残留,小试管中澄清石灰水变浑浊.
碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小刚用如图所示装置进行实验:取少量碳酸氢钠粉末,充分加热后,观察到大试管口有水珠出现,管底有白色固体残留,小试管中澄清石灰水变浑浊.| 操作步骤 | 实验现象 | 结论 |
| 试管内剩余的固体为 Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com