
| A. | 纯铁是具有银白色光泽 | B. | 铁能导电 | ||
| C. | 铁在潮湿的空气中容易生锈 | D. | 铁的密度是7.8克/厘米3 |
分析 物质的化学性质是指在化学变化中表现出来的性质,物质的物理性质是指不需要通过化学变化表现出来的性质.
解答 解:A、纯铁是具有银白色光泽不需要通过化学变化表现出来,属于物理性质,故不符合题意;
B、铁能导电不需要通过化学变化表现出来,属于物理性质,故不符合题意;
C、铁在潮湿的空气中容易生锈需要通过化学变化表现出来,属于化学性质,故符合题意;
D、铁的密度是7.8克/厘米3不需要通过化学变化表现出来,属于物理性质,故不符合题意.
故选:C.
点评 解答本题要分析物质的性质是否需要通过化学变化表现出来,如果需要通过化学变化表现出来就属于物质的化学性质.如果不需要通过化学变化表现出来就属于物质的物理性质.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | 不加二氧化锰就不会产生氧气 | |
| B. | 反应装置中不需要在试管口加棉花 | |
| C. | 用带火星的木条检验生成的气体,木条不复燃 | |
| D. | 发生反应后二氧化锰质量减少 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 空气中氧气体积含量的测定
空气中氧气体积含量的测定查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
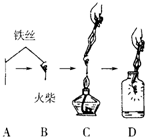 如图是细铁丝在氧气中燃烧实验的操作示意图.请回答下列问题.
如图是细铁丝在氧气中燃烧实验的操作示意图.请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用硫磺熏制白木耳、粉丝等食品 | B. | 用含碳酸氢钠的发酵粉焙制糕点 | ||
| C. | 用聚氯乙烯塑料做食品包装袋 | D. | 用工业石蜡给水果上蜡“美容” |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
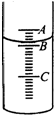 实验室里有一瓶标签残缺的盐酸,请你探究.
实验室里有一瓶标签残缺的盐酸,请你探究.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com