
| A. | 0.8 g | B. | 1.2 g | C. | 1.6 g | D. | 2.4g |
分析 根据将产生的气体通入足量澄清石灰水,生成沉淀0.1mol可得将炭粉、氧化铜和碳酸钙的混合物隔绝空气加强热生成的二氧化碳的质量为0.1mol,假设二氧化碳全是碳粉和氧化铜反应得到的求出碳粉的量为0.1mol,此时碳粉的质量为12×0.1mol=1.2g,而实际生成的二氧化碳还有碳酸钙分解得到的,所以碳粉和氧化铜反应生成的二氧化碳的量小于0.1mol,混合物中碳粉的质量小于1.2g分析.
解答 解:将产生的气体通入足量澄清石灰水,生成沉淀0.1mol可得将炭粉、氧化铜和碳酸钙的混合物隔绝空气加强热生成的二氧化碳的质量为0.1mol,假设二氧化碳全是碳粉和氧化铜反应得到的求出碳粉的量为0.1mol,此时碳粉的质量为12g/mol×0.1mol=1.2g,而实际生成的二氧化碳还有碳酸钙分解得到的,所以碳粉和氧化铜反应生成的二氧化碳的量小于0.1mol,混合物中碳粉的质量小于1.2g,故选A.
点评 解答这类题采用极值法,然后结合题意和化学反应分析即可.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
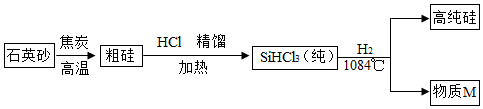
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
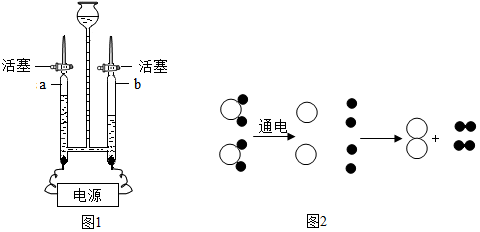
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
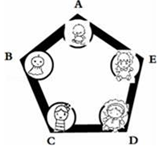 现有五种物质盐酸、硫酸、氢氧化钠、氯化钡和碳酸钠作为某重地的守护“卫士”,只有相邻物质间能发生反应才能组成守护的防线(如图所示),其中物质A常用于铅酸蓄电池中,其浓溶液有脱水性;物质C是人体胃液中的主要成分.(提示:碳酸钡不溶于水)
现有五种物质盐酸、硫酸、氢氧化钠、氯化钡和碳酸钠作为某重地的守护“卫士”,只有相邻物质间能发生反应才能组成守护的防线(如图所示),其中物质A常用于铅酸蓄电池中,其浓溶液有脱水性;物质C是人体胃液中的主要成分.(提示:碳酸钡不溶于水)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com