



 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
| A、火碱和纯碱都属于碱 |
| B、干冰和生石灰都属于氧化物 |
| C、氧气属于纯净物,冰水混合物属于混合物 |
| D、含碳化合物属于有机物,所以CH4、CO、CO2、Na2CO3等都属于有机物 |
查看答案和解析>>
科目:初中化学 来源: 题型:
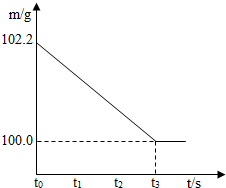 将碳酸钠和硫酸钠的固体混合物12.2g放入烧杯中,再加入一定质量的稀硫酸使其恰好反应,测得反应后所得溶液中溶质质量分数为17.5%,烧杯和所盛物质的总质量(m)与反应时间(t)的关系如图所示.计算:
将碳酸钠和硫酸钠的固体混合物12.2g放入烧杯中,再加入一定质量的稀硫酸使其恰好反应,测得反应后所得溶液中溶质质量分数为17.5%,烧杯和所盛物质的总质量(m)与反应时间(t)的关系如图所示.计算:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com