



科目:初中化学 来源:不详 题型:单选题
| A.用二氧化锰鉴别过氧化氢和蒸馏水 |
| B.用稀盐酸检验某黄金饰品中是否含有铜 |
| C.用闻气味的方法区别一氧化碳和二氧化碳气体 |
| D.用适量的氯化钡溶液除去硝酸钠溶液中的硫酸钠杂质 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验操作 | 测定结果 | 白色固体成分 |
| 用pH试纸测定反应后溶液的酸碱度,操作方法是 | pH>7 | |
| | CaCl2 |
| 部分物质的溶解性表(室温) | ||||
| | OH- | Cl- | SO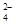 | CO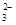 |
| H+ | | 溶、挥 | 溶 | 溶、挥 |
| Ba2+ | 溶 | 溶 | 不溶 | 不溶 |
| Ca2+ | 微溶 | 溶 | 微溶 | 不溶 |
| Mg2+ | 不溶 | 溶 | 溶 | 微溶 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验内容 | 实验现象 | 分析与结论 |
 | 醋酸晶体试管内 (1),醋酸溶液试管中镁带表面冒气泡。 | 酸的很多反应通常在水溶液中才能完成。 |
用玻璃棒蘸硫酸在白纸上写字 | (2)(填“浓”或“稀”)硫酸使白纸炭化。 | 即使是同种酸,由于(3) 不同,它们的性质不完全相同。 |
 | 两试管中均产生(4) | 不同的酸具有相似的性质,这是因为酸的组成中都含有 (5)(填元素符号)。 |
 | E试管中产生 (6) , F试管中无明显现象。 | 不同的酸根会导致酸的“个性”差异。因此,可用氯化钡溶液鉴别盐酸和硫酸。 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 序号 | 实验内容 | 实验现象 | 实验结论 |
| ① | 取少量样品于烧杯中,滴加稀盐酸 | 有大量气泡生成 | 本格不填 |
| ② | 用铂丝蘸取①中溶液,在酒精灯上灼烧 | 火焰为砖红色 | 溶液中含有钙离子 |
| ③ | 另取少量样品于烧杯中,加水充分溶解,滴加 | 无蓝色出现 | 样品中不含有淀粉 |
| ④ | 另取少量样品于烧杯中,加水溶解,静置、过滤,在滤液中加入适量浓硝酸,加热至沸 | __ | 样品中含蛋白粉 (氨基酸) |


查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
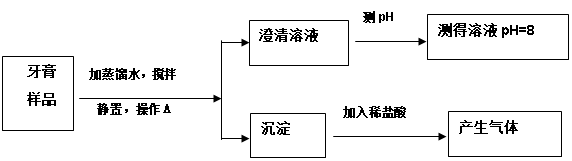
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com