
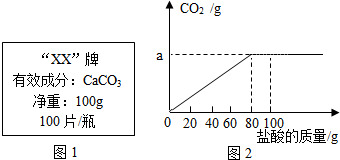
 钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如图2.请根据有关信息回答问题.
钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如图2.请根据有关信息回答问题.| 第1次 | 第2次 | 第3次 | 第4次 | 第五次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 | 20 | 20 |
| 剩余固体的质量(g) | 35 | 30 | m | 20 | n |
分析 (1)根据由第1次和第4次数据可知20g稀盐酸可消耗5g碳酸钙,则第2次加入20g稀盐酸后,剩余固体为30g,第三次加入30g稀盐酸后,剩余固体为25g,故m的数值为25解答;
(2)根据表中信息解答;
(3)根据根据图2可知只有80g盐酸参加反应,根据碳酸钙碳的质量结合化学方程式可计算80g盐酸中氯化氢的质量即可解答.
解答 解:
(1)由第1次和第4次数据可知20g稀盐酸可消耗5g碳酸钙,则第2次加入20g稀盐酸后,剩余固体为30g,第三次加入30g稀盐酸后,剩余固体为25g,故m的数值为25;由表格信息可知,80g稀盐酸与40片药剂中的碳酸钙恰好完全,第5次加入20g稀盐酸后,剩余固体为20g;
由表格信息可知,80g稀盐酸与40片药剂中的碳酸钙恰好完全,消耗碳酸钙20g,40片该药剂的质量=$\frac{40片}{100片}×100g$=40g,该品牌补钙药剂中CaCO3的质量分数是$\frac{20g}{40g}×$100%=50%
设生成二氧化碳的质量为x,第4次加入稀盐酸后,消耗盐酸中的溶质质量为y
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 73 44
20g y x
$\frac{100}{20g}=\frac{73}{y}=\frac{44}{x}$
x=8.8g
y=14.6g
该盐酸中溶质的质量分数为$\frac{14.6g}{80g}$×100%=18.3%;
故答案为:
(1)25 20
(2)50%;8.8;
(3)该盐酸中溶质的质量分数为18.3%
点评 本题主要考查学生运用化学方程式进行和质量分数公式进行计算的能力.


科目:初中化学 来源: 题型:选择题
| A. | 提倡骑自行车或步行等方式出行 | |
| B. | 购物时尽量使用无纺布袋,少用一次性塑料袋 | |
| C. | 油菜、小麦收割后,用粉碎机将秸秆粉碎并填埋在田间 | |
| D. | 油菜、小麦收割后将秸秆就地焚烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 含碳元素的物质一定是有机物 | |
| B. | 同种元素组成的物质一定不是化合物 | |
| C. | 铵态氮肥可与碱性物质混合使用 | |
| D. | 向某物质中滴加稀盐酸,冒气泡,则该物质一定是碳酸盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 预计现象 | 预计结论 |
| 取少量反应后的溶液于试管中,逐滴加入碳酸钠溶液. | 只有白色沉淀产生 | 猜想(B)正确 |
| 先有气泡产生,后有白色沉淀产生 | 猜想(C)正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
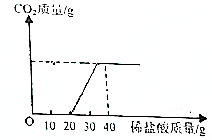 某造纸厂排放的废水中含有Na2CO3和NaOH,为测定废水中Na2CO3的质量分数,取50g废水样品于烧杯中,将40g稀盐酸分成4等份分4次慢慢加入到烧杯中,获得的实验现象和数据如表所示:
某造纸厂排放的废水中含有Na2CO3和NaOH,为测定废水中Na2CO3的质量分数,取50g废水样品于烧杯中,将40g稀盐酸分成4等份分4次慢慢加入到烧杯中,获得的实验现象和数据如表所示:| 实验次数 | 1 | 2 | 3 | 4 |
| 稀盐酸的质量(g) | 10 | 10 | 10 | 10 |
| 生成气体质量(g) | 0 | x | 1.2 | 1.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com