
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:初中化学 来源: 题型:
| A、硫在氧气中燃烧产生明亮的蓝紫色火焰 |
| B、消防队员用水降低可燃物的温度来灭火 |
| C、排水集气法:当导管口刚有气泡冒出时,还不能收集气体 |
| D、合金的硬度比组成它们的纯金属的硬度小 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、析出晶体后的此溶液是该温度下此物质的饱和溶液 |
| B、饱和溶液一定是浓溶液 |
| C、同一溶质的饱和溶液一定比它的不饱和溶液浓度大 |
| D、降低温度,不饱和溶液一定可以变为饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:
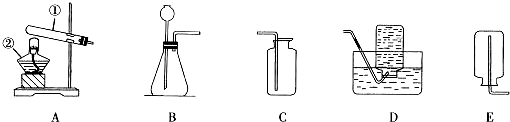
查看答案和解析>>
科目:初中化学 来源: 题型:
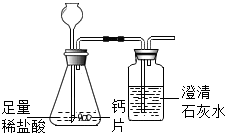
| 钙片质量 | 空洗气瓶质量 | 澄清石灰水的质量 | 反应后洗气瓶及瓶内物质总质量 |
| 20g | 100g | 200g | 300.4g |
| 加入稀盐酸的质量/g | 100 | 200 | 300 | 400 |
| 充分反应后烧杯及杯内物质总质量/g | 217.8 | a | 413.4 | 513.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com