
| A. | 加热 | B. | 降温 | ||
| C. | 加硝酸钾固体 | D. | 加该温度下的硝酸钾饱和溶液 |
分析 饱和溶液是指在一定温度下、一定量的溶剂里,不能再继续溶解这种溶质的溶液,进行分析解答.
解答 解:A、硝酸钾的溶解度随着温度的升高而增大,加热后温度升高,硝酸钾的溶解度增大,不能证明原硝酸钾溶液是否饱和,故选项错误.
B、硝酸钾的溶解度随着温度的降低而减小,接近饱和的溶液降低温度也可能有晶体析出,不能证明原硝酸钾溶液是否饱和,故选项错误.
C、加硝酸钾固体,硝酸钾不能继续溶解,说明原溶液为该温度下的饱和溶液,故选项正确.
D、加该温度下的硝酸钾饱和溶液,不能证明原硝酸钾溶液是否饱和,故选项错误.
故选:C.
点评 本题难度不大,是对饱和溶液概念的理解,理解饱和溶液是指在一定温度下、一定量的溶剂里,不能再继续溶解这种溶质的溶液是解题的关键.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
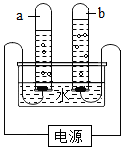 如图是电解水的简易装置.看图填空:
如图是电解水的简易装置.看图填空:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 它的俗名叫生石灰,水溶液叫石灰水 | |
| B. | 它是一种白色粉末状固体,易溶于水 | |
| C. | 它的溶液能使紫色石蕊试液变成蓝色,使无色酚酞试液不变色 | |
| D. | 它能与碳酸钠溶液反应,来制备火碱 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com