
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:初中化学 来源: 题型:选择题
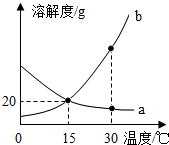 a、b两种物质的溶解度曲线如图所示.下列说法不正确的是( )
a、b两种物质的溶解度曲线如图所示.下列说法不正确的是( )| A. | 15℃时,a、b的溶解度均为20g | |
| B. | 加水或升温均可使b的饱和溶液变为不饱溶液 | |
| C. | 30℃时,向100g水中加入20g a,可得120g溶液 | |
| D. | 将30℃时a的饱和溶液降温至15℃,溶质的质量分数不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 正在建设的哈尔滨地铁2号线为哈市今后的经济发展及交通畅通将发挥重要的作用,下列说法正确的是( )
正在建设的哈尔滨地铁2号线为哈市今后的经济发展及交通畅通将发挥重要的作用,下列说法正确的是( )| A. | 地铁建设中使用了许多生铁、钢、水泥等金属材料 | |
| B. | 地铁车厢的外壳用的是铝合金,与纯铝相比,具有密度小、熔点高、抗腐蚀性好的性质 | |
| C. | 地铁的钢轨是用质量较好的不锈钢制造,具有硬度大,抗腐蚀性好的优点 | |
| D. | 地铁站采用了节能照明设备,降低了能源消耗,有利于节能环保 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
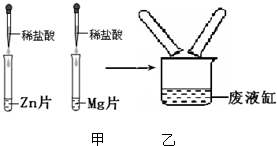 在甲、乙两支试管中分别加入等质量的金属锌片和镁片,再加入等质量、等质量分数的稀盐酸,充分反应后,甲试管中盐酸过剩,乙试管中镁片过剩,将两试管中剩余物都倒入废液缸中,充分混合后固体消失,废液缸溶液中没有任何不溶物.
在甲、乙两支试管中分别加入等质量的金属锌片和镁片,再加入等质量、等质量分数的稀盐酸,充分反应后,甲试管中盐酸过剩,乙试管中镁片过剩,将两试管中剩余物都倒入废液缸中,充分混合后固体消失,废液缸溶液中没有任何不溶物.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
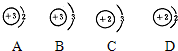
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
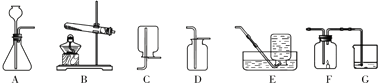
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com