
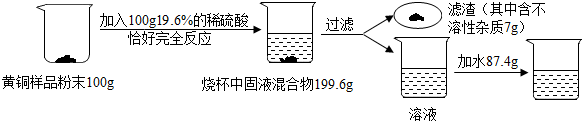
分析 (1)根据溶液稀释前后,溶质质量不变进行分析;
(2)根据质量守恒定律计算生成氢气的质量,然后依据化学方程式计算参加反应的锌的质量,然后计算铜的质量分数;
(3)根据化学方程式和题中的数据计算生成硫酸锌的质量,然后计算溶质的质量分数.
解答 解:(1)需要溶质质量分数为98%的浓硫酸的质量是:$\frac{100g×19.6%}{98%}$=20g;
(2)生成氢气的质量为:100g+100g-199.6g=0.4g
设参加反应的锌的质量为y,生成硫酸锌的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 161 2
x y 0.4g
$\frac{65}{x}$=$\frac{161}{y}$=$\frac{2}{0.4g}$
x=13g
y=32.2g
所以$\frac{100g-13g-7g}{100g}$×100%=80%;
(3)最终所得溶液的溶质质量分数为:$\frac{32.2g}{199.6g-80g-7g+87.4g}$×100%=16.1%.
故答案为:(1)20g;
(2)80%;
(3)16.1%.
点评 本题主要考查了根据化学方程式的计算,要想解答好这类题目,就要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的物质的质量等知识.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:初中化学 来源: 题型:解答题
 环境和食品安全卫生管理,关系百姓身体健康,也是重要的社会民生问题.
环境和食品安全卫生管理,关系百姓身体健康,也是重要的社会民生问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| NaHCO3 | Na2CO3 | |
| 加人稀盐酸 | 现象Ⅰ | 产生气泡 |
| 加人饱和石灰水 | 溶液变浑浊 | 现象Ⅱ |
| 加人CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
| 加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
| 实验步骤 | 实验现象 | |
| ①取少量样品溶于水,加人过量 的CaCl2溶液. | 有白色沉淀产生 | 该反应的方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl |
| ②将上述反应后的混合液过滤,取滤液. | 有气泡冒出 | 证明猜想②成立. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 马蹄飞燕为东汉青铜器,1969年出土于甘肃省武威雷台的东汉墓,现藏于甘肃省博物馆,1983年10月,马蹄飞燕被国家旅游局确定为中国旅游标志,1986年被定为国宝级文物.
马蹄飞燕为东汉青铜器,1969年出土于甘肃省武威雷台的东汉墓,现藏于甘肃省博物馆,1983年10月,马蹄飞燕被国家旅游局确定为中国旅游标志,1986年被定为国宝级文物.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论及反应方程式 |
| 向滴有酚酞溶液的稀氢氧化钠溶液的试管中,加入稀硫酸,并振荡 | 观察到溶液由红色变为无色 | 氢氧化钠和硫酸发生了反应,反应的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O |
| 实验步骤 | 预期实验现象 | 实验结论 |
| 取(1)实验后溶液少量于试管中,加入锌粒 | 有气泡产生 (或没有气泡产生) | 猜想三(或一)正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 5.6g | B. | 2.8g | C. | 0.4g | D. | 无法计算 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 烧碱属于碱,故纯碱也属于碱 | |
| B. | 生铁比纯铁硬,故黄铜比纯铜硬 | |
| C. | 稀硫酸和稀盐酸是不同的酸,故化学性质完全不同 | |
| D. | 厨房洗涤剂对油污有乳化作用,故汽油对油污也有乳化作用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com