
实验探究一:课本第二单元课后作业中有“寻找新的催化剂” 的探究内容,实验中学探究小组据此设计了如下探究方案。
(提出问题)红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
(实验探究)
实验步骤 | 实验现象 | 实验结论及解释 |
Ⅰ. | A中无明显现象, B中产生大量能使带火星木条复燃的气体 | ① 产生的气体是______ ② 红砖粉末能改变过氧化氢分解速率 |
Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ① 又产生大量能使带火星木条复燃的气体 ② 滤渣质量等于ag | 红砖粉末的_____在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
Ⅲ. | 两试管中均产生气泡且______ | 红砖粉末的催化效果没有二氧化锰粉末好 |
(拓展应用)
己知CuSO4也可作为过氧化氢分解的催化剂。向101.2g一定溶质质量分数的过氧化氢溶液中加入2g CuSO4粉末,充分反应后得到溶质质量分数为2%的溶液,则生成氧气_____g。
实验探究二:实验室中的试剂一般要密封保存,否则可能会与空气接触而变质。淅河中学化学学习小组发现一瓶未密封的氢氧化钾固体,对其是否变质进行探究。
(提出猜想)1.未变质 2.部分变质 3.完全变质
(查阅资料)KOH与NaOH性质类似,也能与CO2反应而变质。写出KOH变质的化学方程式为_____。
(设计实验)
(l)取少量样品于试管中配成溶液,滴加足量稀盐酸有气泡产生,则猜想_____不成立。
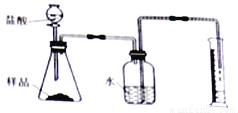
(2)准确称取一定质量的固体样品,放在右图所示装置中进行实验,根据CO2的体积和密度计算变质产物的质量,从而确定变质情况,你认为这个方案是否可行,并说明理由_________。
(3)请你另外设计一个方案,进一步探究变质情况
实验步骤 | 实验现象 | 实验结论 |
______________ | _____________ | 猜想2成立 |
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源:山东省威海市业考试模拟训练化学试卷 题型:科学探究题
“贝壳变废为宝”的实验探究
我们知道贝壳中含有碳酸钙,威海每年都会产生大量被废弃的贝壳,如果有效加以利用不但可以变废为宝,而且还能保护环境,某兴趣小组以此展开探究:
探究问题:贝壳中碳酸钙的含量是多少?
(1)设计定量实验来探究贝壳中主要成分碳酸钙的含量。
实验方案如下:称取1克贝壳,放入盛有一定量的盐酸的烧杯中,将气体通入氢氧化钠溶液中,测量氢氧化钠溶液增重的质量,即为二氧化碳的质量,进而求得碳酸钙的含量。小姜认为该实验方案不严密,会造成实验测定结果不准确,你赞同吗?_________,请尽可能考虑多种情况,从方案设计及对应的实验测定结果两方面阐述你的理由_________________________。
(2)如果给你一份未知浓度的稀盐酸,要求通过定量实验来测定贝壳中碳酸钙的含量,请写出具体的实验方案。
实验方案 | 反应的化学方程式 |
_____________ | ________________ |
查看答案和解析>>
科目:初中化学 来源:北京市朝阳区2018届九年级综合练习(二)化学试卷 题型:流程题
MnCO3用作涂料和清漆的颜料。MnCO3不溶于水,100℃时开始分解。以软锰矿(主要成分MnO2)为原料制备高纯MnCO3的流程如下:
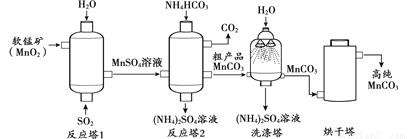
(1)反应塔1中的反应为:MnO2+SO2==MnSO4,其中化合价发生改变的元素是________。
(2)洗涤塔中喷水的目的是__________。
(3)烘干塔中需选择“低温”干燥的原因是_______________。
(4)上述流程中的产品除高纯MnCO3外,还有______________。
Mn、S 除去粗产品MnCO3中的(NH4)2SO4 防止MnCO3高温分解 (NH4)2SO4溶液、CO2 【解析】(1)反应前锰元素的化合价是+4,反应后锰元素的化合价是+2,反应前硫元素的化合价是+4,反应后硫元素的化合价是+6。(2)MnCO3不溶于水,而(NH4)2SO4易溶于水,所以洗涤塔中喷水的目的是除去粗产品MnCO3中的(NH4)2SO4。(3)烘干塔中需选择“低温”干燥的...查看答案和解析>>
科目:初中化学 来源:北京市朝阳区2018届九年级综合练习(二)化学试卷 题型:单选题
下列方法能鉴别空气、氧气和二氧化碳3瓶气体的是
A. 闻气味 B. 将集气瓶倒扣在水中
C. 观察颜色 D. 将燃着的木条伸入集气瓶中
D 【解析】要同时鉴别三种物质,那么要产生三种不同的现象。 三种气体都是无色无味的,错误; 空气和氧气均难溶于水,二氧化碳易溶于水,只能将二氧化碳鉴别出来,错误; 三种气体均是无色的,错误; 将燃着的木条伸入装有空气的集气瓶中,燃着的木条无明显变化;燃着的木条伸入氧气中,燃着的木条伸入燃烧的更旺;燃着的木条伸入二氧化碳中,燃着的木条会熄灭,正确。 故选D。 ...查看答案和解析>>
科目:初中化学 来源:专题15 科学探究(中考题)-决胜2018中考化学压轴题全揭秘精品 题型:填空题
有一包白色固体样品,可能含碳酸钠、硫酸钠、氯化钠、氢氧化钠中的一种或几种。小科同学为探究其成分做了以下实验:

Ⅰ.取少量固体样品于烧杯中,先加足量水溶解,再加入足量的BaCl2溶液,有白色沉淀产生;
Ⅱ.继续向烧杯中滴加稀盐酸并不断搅拌,烧杯内固体质量随加入稀盐酸质量的变化如图所示。
请回答下列问题:
(1)AB段观察到的现象是 。
(2)C点时,溶液中一定含有的溶质是 。
(1)固体部分溶解并有气泡产生 (2)NaCl、BaCl2、HCl 【解析】(1)AB段沉淀质量减少,说明加入稀盐酸后沉淀部分溶解并生成气体。故AB段观察到的现象是:固体部分溶解并有气泡产生; (2)加入稀盐酸后沉淀部分溶解,说明加入BaCl2溶液生成碳酸钡沉淀和硫酸钡沉淀。在生成沉淀的同时生成氯化钠。稀盐酸与碳酸钡反应生成氯化钡。又C点时稀盐酸过量。故C点时,溶液中一定含有的溶...查看答案和解析>>
科目:初中化学 来源:黑龙江省绥化市绥棱县2018届九年级(五四学制)下学期第六次月考化学试卷 题型:综合题
热水瓶用久后,瓶胆内壁常附着一层水垢,其成分是碳酸钙、氢氧化镁及少量水,实验室现有一瓶水垢样品,为测定其中各成份的质量分数,某化学兴趣小组的同学利用如图所示装置进行实验(该装置气密性良好,A、C、D中所装药品足量)。
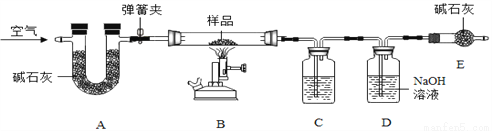
已知:碱石灰是氧化钙和氢氧化钠的混合物;加热条件下,氢氧化镁易分解,反应的化学方程式为:Mg(OH)2 △ MgO+H2O↑。
部分实验步骤如下:
Ⅰ.将质量为m的样品装入装置B的玻璃管中,按图连接好装置,关闭弹簧夹,给样品加热;
Ⅱ.待样品完全反应,先打开弹簧夹通入空气,再熄灭酒精喷灯,直到玻璃管冷却;
Ⅲ.实验完毕,测得装置C、D中的液体质量分别增加了m1、m2;
Ⅳ.根据实验所测数据计算该样品中碳酸钙、氢氧化镁和和水的质量分数。
请回答下列问题:
(1)装置C中所装药品为_____________,其作用是___________________。
(2)装置D中发生反应的化学方程式为______________________________。
(3)该水垢样品中碳酸钙的质量分数表达式为________________________。
(4)实验反思:实验步骤不变,若没有装置A,会导致氢氧化镁的测定结果______(填“偏大”、“偏小”或“无法判断”)。
(5)若除去热水瓶胆内壁常附着的水垢,可以用厨房中的______________。
浓硫酸 吸水干燥气体 2NaOH+CO2===Na2CO3+H2O {2500m2/11m}% 偏小 食醋 【解析】(1)氢氧化镁在加热条件下分解生成氧化镁和水,碳酸钙在高温条件下分解生成二氧化碳和氧化钙,由生成二氧化碳的质量可计算水垢中的碳酸钙的质量。装置C中所装药品为浓硫酸,其作用是吸水,干燥气体二氧化碳;(2)装置D的作用是吸收二氧化碳,发生反应的化学方程式为2NaOH+CO2===N...查看答案和解析>>
科目:初中化学 来源:黑龙江省绥化市绥棱县2018届九年级(五四学制)下学期第六次月考化学试卷 题型:填空题
下图是氢气和氧气发生反应的微观模拟图,请回答下列问题:

(1)在B图中将相关粒子图形补充完整;____________
(2)A图所示物质属于____________(填物质分类),从微观角度说明理由___________
(3)画出一个具有相对稳定结构的原子结构示意图___________________。
、 混合物 由两种分子构成 【解析】(1)据质量守恒定律可知,反应前后原子的种类、个数不变,氢气燃烧时,每两个氢分子和一个氧分子结合生成两个水分子;在B图中应补充一个和一个;(2)A图所示物质由两种物质组成,属于混合物,微观角度的理由是:物质由两种分子构成;(3)在原子结构示意图中,小圆圈表示原子核,圆圈内的数字为质子数;弧线表示电子层,弧线上的数字为该层上的电子数。原子核外只有一个电子层且...查看答案和解析>>
科目:初中化学 来源:黑龙江省绥化市绥棱县2018届九年级(五四学制)下学期第六次月考化学试卷 题型:单选题
.哈尔滨大街小巷有许多的营养早餐车。下列食品中富含营养素种类最多的是
A. 油条 B. 大米粥 C. 面包 D. 汉堡 ( )
D 【解析】A. 油条提供的营养素主要有糖类,油脂; B. 大米粥提供的营养素主要是糖类; C. 面包提供的营养素主要糖类; D. 汉堡提供的营养素主要有糖类、油脂、蛋白质、维生素等;故选D。查看答案和解析>>
科目:初中化学 来源:内蒙古赤峰市2018届九年级中考模拟化学试卷 题型:简答题
某公司生产出的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。
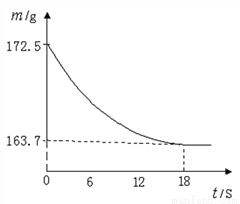
求:(1)生成CO2的质量为__________g。
(2)该纯碱样品中Na2CO3的质量分数为________。
8.8 80% 【解析】试题分析:(1)根据质量守恒定律可知,减少固体的质量即为产生二氧化碳质量;(2)根据二氧化碳质量,利用化学方程式进行计算得出碳酸钠质量,再用碳酸钠质量除以样品质量即可。具体步骤如下: 【解析】 (1)生成二氧化碳质量=172.5g-163.7g=8.8g (2)设该纯碱样品中碳酸钠质量为X Na2CO3+2HCl==2NaCl+H2O+CO2↑ ...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com