

分析 (1)中和反应是酸与碱起反应生成盐和水的反应,海水中的氯化镁浓度较低,结合提取镁的过程进行分析解答有关的问题;
(2)①根据海水晒盐的方法及结晶的方法进行分析解答;
②氯化镁可以和氢氧化钠溶液反应生成沉淀,但是氯化钠不能和氢氧化钠溶液反应,可以据此进行解答;
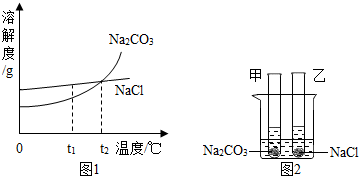
(3)①根据溶解度曲线的意义进行解答;
②根t2℃时,Na2CO3和NaCl的溶解度相等进行解答;
③根据碳酸钠和氯化钠的溶解度受温度变化影响的大小进行解答.
解答 解:(1)由提取镁的过程可知,反应②中氢氧化镁和稀盐酸反应生成氯化镁和水,属于酸与碱发生了反应生成了盐和水,属于中和反应;海水中含有的氯化镁浓度较低,加入石灰乳变为氢氧化镁沉淀,过滤后加入盐酸制备氯化镁,再经过蒸发干燥制备无水氯化镁,最后经过通电可制得镁;通过前两步反应我们将氯化镁富集起来.
故答案:Mg(OH)2+2HCl=MgCl2+2H2O;将氯化镁富集起来.
(2)①海水晒盐是利用了蒸发溶剂的方法得到食盐晶体,即通过风吹日晒使水分蒸发从而得到食盐晶体,分析所给的选项可以知道选项B正确,故选B;
②氯化镁可以和氢氧化钠溶液反应生成沉淀,但是氯化钠不能和氢氧化钠溶液反应,所以可以用氢氧化钠溶液来进行检验,即向溶液中加入适量NaOH溶液,出现白色沉淀,则证明有MgCl2;
故答案为:B;向溶液中加入适量NaOH溶液,出现白色沉淀,则证明有MgCl2;
(3)①根据溶解度曲线的意义可以知道在t1℃时,Na2CO3的溶解度小于NaCl的溶解度;
②t2℃时,的Na2CO3和NaCl的溶解度相等,因此相同质量的Na2CO3和NaCl的饱和溶液中所含溶质的质量也相等;
③从溶解度曲线可以得出碳酸钠的溶解度受温度变化影响比较大,所以若向试管外盛有水的烧杯中加入某物质后,甲试管中固体明显减少,而乙试管中的固体无明显减少,则加入的物质可能是溶液的温度升高,根据所学知识可以知道,加入的物质可以是氢氧化钠等物质.
故答案为:①小于;
②相等;
③NaOH等(合理即可).
点评 本题以海洋为知识载体,重点考查了溶解度曲线的应用、反应原理的分析及方程式的书写,要学会从问题中寻求对信息的有效解读和捕捉,这样能够提高问题的解决的速度和准确度.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
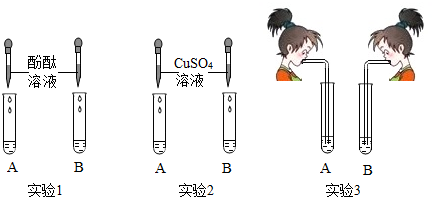
| 实验 | 实验现象 | 结论 |
| 取B中少量溶液,加入澄清石灰水至不再产生沉淀为止,过滤后取上层清液,向其中加几滴酚酞试液 | 产生白色沉淀溶液呈现红色 | 猜想3成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 混合物一定由不同种物质构成 | |
| B. | 有单质生成的反应一定是置换反应 | |
| C. | 只含有一种元素的物质一定是纯净物 | |
| D. | 在溶液中,只有固体和液体可以作为溶质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 在化学反应中一般易失电子 | B. | 该粒子呈电中性 | ||
| C. | 其表示的元素在化合物中常显+3价 | D. | 化学性质较稳定 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | C2H5OH(酒精)和NaCl 溶液(闻气味) | B. | NaOH溶液和稀H2SO4 溶液(酚酞试液) | ||
| C. | Ca(OH)2溶液和NaOH溶液(稀盐酸) | D. | KMnO4 和KClO3 (观察颜色) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 7.6g气体全部是O2 | |
| B. | 7.6g气体通过足量NaOH溶液后,气体减少4.4g | |
| C. | 反应后的固体是混合物 | |
| D. | 生成Na2CO3的质量为31.8g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com