



科目:初中化学 来源:321创新实践同步单元练习与测素质教育 题型:058
碱石灰是一种常用的干燥剂,它可由固体NaOH和CaO混合而成的,它极易吸收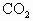 和水.工业用纯碱中常混有杂质NaCl,实验室中可以利用下列装置测定该纯碱中
和水.工业用纯碱中常混有杂质NaCl,实验室中可以利用下列装置测定该纯碱中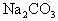 的质量分数.
的质量分数.
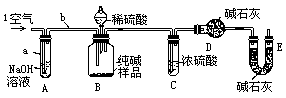
实验步骤如下:
①准确称取w g纯碱样品,置于B装置中.
②向B装置中滴加稀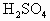 ,同时从“1”处缓缓地鼓入空气,直至B中不再产生气体为止.
,同时从“1”处缓缓地鼓入空气,直至B中不再产生气体为止.
(1)写出图中仪器a、b的名称:a________,b________.
(2)写出装置B中发生反应的化学方程式:________.
(3)从“1”处缓缓地鼓入空气的目的是________.
(4)A装置的功用是________.
(5)C装置的功用是________.
(6)实验前称量D装置的质量是m g,实验后称量D装置的质量是n g.该纯碱样品中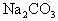 的质量分数是________(用含m、n、w的式子表示).
的质量分数是________(用含m、n、w的式子表示).
(7)E装置的功用是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com