
����Ŀ����ͼ�dz������ʵ�ת����ϵ������X��Ũ��Һ�ܻӷ����ݼ�����ζ�����壬A��D �ķ�Ӧ����������ɫ�������ɣ�EΪ��ɫ���������ַ�Ӧ������P��Ӧ������ʡ�ԡ�
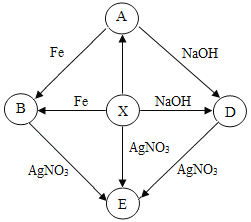
��1��B�Ļ�ѧʽΪ_____��
��2��д��X��D�Ļ�ѧ����ʽ_____��
��3��E�Ļ�ѧʽΪ_____��X��AgNO3��Ӧ��������Һ��pH_____7��ѡ����ڡ�С�ڻ��ڡ�����
��4��A��Һ�����۳�ַ�Ӧ��ȡʣ�����������ᣬû������ų�����A�����۷�Ӧ�����Һ����г��� H2O������B�⣬�����ܴ��ڵ�������_____��д��ѧʽ����
���𰸡�FeCl2 NaOH+HCl=NaCl+H2O AgCl �� CuCl2
��������
����A��G�dz��л�ѧ�������ʣ�X��Ũ��Һ�ܻӷ����̼�����ζ�����壬X�����ۡ��������ƻᷴӦ������X�����ᡣ��A��D�ķ�Ӧ����������ɫ�������ɣ����ݸ��ֽⷴӦԭ����֪A�к���ͭ���ӣ�A����ͭ�Σ���A������X����ת����������A���Ȼ�ͭ���Ȼ�ͭ���������Ʒ�Ӧ������ɫ��������ͭ�������Ȼ��ƣ�������������Ʒ�ӦҲ�������Ȼ��ƺ�ˮ������D���Ȼ��ơ��Ȼ�ͭ�����۷�Ӧ�������Ȼ�������ͭ�����������Ӧ�������Ȼ�����������������B���Ȼ�������EΪ��ɫ������X��B��D�ж����������ӣ�����������Ӧ�����ɰ�ɫ����������E���Ȼ�����
��1�����ݷ�����֪��B�������Ȼ��������ʴ�Ϊ��FeCl2��
��2�����ݷ�����֪��X��D�ķ�Ӧ��������������Ʒ�ӦҲ�������Ȼ��ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪNaOH+HCl=NaCl+H2O���ʴ�Ϊ��NaOH+HCl=NaCl+H2O��
��3�����ݷ�����E�Ļ�ѧʽΪ AgCl��X��AgNO3��Ӧ����ϡ��������������Һ��Ӧ�����Ȼ���������ϡ���ᣬ���������ԣ��ʷ�Ӧ��������Һ��pH��7���ʴ�Ϊ��AgCl������
��4��ͨ���Ƶ���֪A���Ȼ�ͭ���Ȼ�ͭ��Һ�����۷�Ӧ��ȡʣ�����������ᣬû������ų���˵����Ӧ��Ĺ�����û�����ۣ����ۿ��ܸպ����Ȼ�ͭ��Ӧ����ʱ��Һ�е��������Ȼ��������п������۲��㣬û�����Ȼ�ͭ��ȫ��Ӧ����ʱ��Ӧ����������Ȼ��������Ȼ�ͭ������A�����۷�Ӧ�����Һ����г���H2O�⣬һ�����ڵ�������FeCl2�����ܴ��ڵ�������CuCl2���ʴ�Ϊ��CuCl2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʦ��ָ���£�С��ͬѧ̽������������Һ��Ӧʱ�����ֽ��Ʒ���MgCl2��Һ�������ݺͰ�ɫ����������Ϊ�˽�һ��̽����С��ͬѧ����ַ�Ӧ��Ļ������ˣ��ù���A����ҺB��
���������ϡ�
������ˮ��Ӧ�����������ƺ�������
��MgCl2��Һ��������
��������˼����
С��ͬѧ������ѧ֪ʶ�Բ������������A�����жϣ�
��1�������������� ������ţ���
��CO2 ��H2 ��Cl2
��2��ȡA�������ϡ���ᣬAȫ���ܽ⣬�����ݲ�������A�Ļ�ѧʽ�� ��
��������⡿��ҺB�����ʵijɷ���ʲô��
����һ��NaCl
�������NaCl��MgCl2
��������NaCl��NaOH
�����ģ�NaCl��MgCl2��NaOH
С��ͬѧ��Ϊ���� �������������� ��
��ʵ��̽����
ʵ����� | ʵ������ | ʵ����� |
����һ��ȡ������ҺB���Թ��У��μӼ�����ɫ��̪�����۲����� | ��Һ | ������������ |
�������ȡ������ҺB���Թ��У��μ�����NaOH��Һ�����۲����� | ������ɫ���� | ���� ���� |
�����ۡ��ڽ������˳����Ʋ��ܽ�λ��������Ľ����Ӹý���������Һ���û�������
����չ��������MgCl2��������������ȵ�һ���¶�ʱ���ƿ��Դ�MgCl2���û���þ���÷�Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǻ�ѧʵ���ҳ��õļ���װ�ã��ش��������⣺
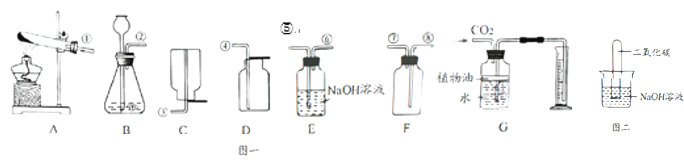
(l)д����װ��A��ȡO2�Ļ�ѧ����ʽ_____��Aװ�����Թܿ���������б��ԭ����_____��
(2)ijͬѧ��Ũ��Ϊ20%��H2O2��Һ��MnO2��ȡ����ʱ��ѡ��װ��Bʵ��ʱ���֣����ܵõ�ƽ�ȵ�����������Ӧ����̫�죩����������Ľ�����_____��
(3)ʵ������ȡCO2,����װ��G�������ռ�CO2������������һ��ֲ���͵�Ŀ����_____��
(4)��һֻ����CO2���Թܵ������ձ�����ͼ����ʾ����֤��CO2����NaOH��Һ��Ӧ����Ӧ��һ���Ա�ʵ����_____��
(5)ͨ���������Ͽ�֪�����ڳ����£������������ƹ������Ũ�����ᷴӦ��ȡSO2,��Ӧԭ��ΪNa2SO3+H2SO4=Na2SO4+H2O+SO2��:��ͨ��״���£�SO2��һ����ɫ���д̼�����ζ���ܶȱȿմ���ж����壬������ˮ��ˮ��Һ�����ԣ�SO2�������Һ��Ӧ��
������ͼһװ����ȡ���ռ�һƿSO2���壬�ҷ�������ɫ��ѧ�������ѡװ�õ�����˳����������ҵķ����ǣ�_____
A �ٽӢ� B �ٽӢޣ��ݽӢ� C �ڽӢ࣬�߽Ӣ� D �ڽӢ�
�ڸ�ʵ����β�������ķ����ǽ�SO2ͨ��NaOH��Һ�У�д����Ӧ�Ļ�ѧ����ʽ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������dz��л�ѧ��Ҫ��ѧϰ������
��1����ѧ��һ����ʵ��Ϊ��������Ȼ��ѧ�����л�ѧ���ϵ�����ʵ����ˮ����������Ҫ��ɫ��

��Χ����ˮ����������������ʵ��ѡ���������ֹ�Ϊһ�࣬ѡ���ʵ����_____������ĸ���������������_____��
��2�����ֽⷴӦ���۱���ʵ���������ӻ�����Ӧ���������ӽ�ϳɳ����������ˮ����Ӧ�Ϳɷ��������෴ӦҲ�������ӷ���ʽ����ʾ�����磬�������ƺ����ᷢ���кͷ�Ӧ���۱��ʿ��Ա�ʾΪ��H++OH-=H2O������������Һ��ϡ���ᷴӦ�ķ���ʽΪ_____�����ӷ���ʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ů������������Ҫ�ɷ�Ϊ���ۣ���������Դ�����۵���ʴ��Ӧ���á�ů���������ⶨ�����������ĺ�����ʵ�鿪ʼǰװ����ͼ��ʾ��ʵ������Ͳ�н��뼯��ƿ���ݻ�Ϊ 250mL����ˮ�����Ϊ45mL��������ʴ���ĵ�ˮ���Բ��ƣ�����������������ǣ�������
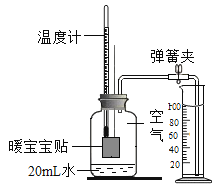
A.ʵ��ǰ������װ�õ�������
B.����ʵ���ÿ������������������Ϊ18%
C.����ÿ�������������ƫ�ͣ����������۲���
D.������¶ȼƵĶ����ָ���ʵ��ǰ���¶Ⱥ��ܼ�¼��Ͳ��ʣ��ˮ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ������ƿ�г���������̼,���ձ���ȼ��2֧�ߵͲ��ȵ�����ʵ��ʱ��ֹˮ�У��ƿ�����Ƭ������˵����ȷ���ǣ�������
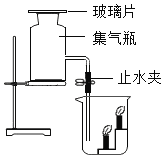
A.���۲쵽�ߵ�������Ϩ��
B.���ƿ�����Ƭ��ʵ�����������
C.�����Ϩ������Ϊ������̼������������Ż��
D.ȥ���ձ��е�1֧����,Ҳ�ܵó�ͬ����ʵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������벻��������

��1������������Ʒ�У���Ҫ���ý��������Ե���____________������ĸ����
��2��2019 �� 8 �� 30 �գ��°����������ҷ��У����� 5 ��Ӳ�ҵIJ�����ԭ���ĸ�о��ͭ�Ͻ��Ϊ��о�����Ͻ�ѡ������Ӳ�ҵIJ��ϲ���Ҫ���ǵ�������_________������ţ���
A�����ĵ����� B��������ʴ�� C������Ӳ�� D�����۸���Ӳ����ֵ���Ǻ϶�
��3������Ӧ����㷺�Ľ����������ڴ���ս��ʱ�ڣ��ҹ��Ŵ������Ѿ���ʼ������д���������� CO��Ӧ�Ļ�ѧ����ʽ___________��
������������Ʒ�������⣬�û�ѧ����ʽ��ʾ�����ԭ����__________��
��Ŀǰ���������� 50%���ϵĸ����õ��������ã���Ŀ����__________������ţ���
A��Լ������Դ B�������ɿ��� C��ֹ��������
��4���� AgNO3��Cu(NO3)2�Ļ����Һ�м���һ����п�ۣ���ַ�Ӧ����ˣ�����������Һ������Һ����ɫ����������һ�����е�������____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1������ͼʾʵ��װ�ã��ش��������⡣
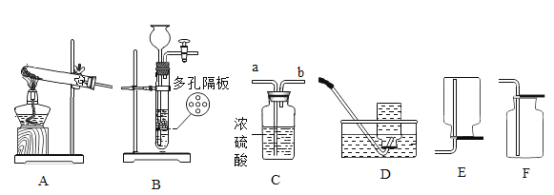
��ʵ�����ø��������ȡ����������װ��Ӧѡ������װ����___________�����ţ������ù���������Һ��ȡ�����������װ�ú���������˳��Ϊ������װ����C��___________�����ţ�������װ��ʱ������װ�õij�����Ӧ��װ��C��_____________������a������b������������
��ʵ����ʹ��Bװ����ȡ������̼��ͻ���ŵ���____________�����ƵõĶ�����̼ͨ����ɫʯ����Һ�У��۲쵽��������_____________��
��2��ij��ѧ��ȤС����ʯ��ʯ��������ȡһƿCO2������������ʯ��ˮ���뼯��ƿ�У�����û�б���ǡ���ȤС�������쳣���������̽����
��������⣩����ʯ��ˮΪʲôû�б���ǣ�
����������]��CO2����ʱ��CaCO3������ת��Ϊ������ˮ��Ca��HCO3��2��
��AgCl������ϡ����
��������룩I.ʯ��ˮ����ȫ���� ��_______.��.CO2�л���HCl
��ʵ�鷽������ȤС����ԭҩƷ������ȡCO2��������̽����
�Ʊ�CO2�Ļ�ѧ����ʽΪ___________��
ʵ�鲽�� | ʵ������ | ʵ����� |
1.ȡ��������ʯ��ˮ���Թ��У�����________��Һ�� | ������ɫ���� | ����I������ |
2.����������ͨ��ʢ�г���ʯ��ˮ���Թ��� | __________ | ������������ |
3.____________ | ______________ | ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��������ͼ��ʵ��װ�ã��ش����⣺
����װ�� | �ռ�װ�� | ϴ��װ�� |
|
|
|
��ͼB������a������_____��
��ʵ�����ü�������غͶ������̻������ȡ�����Ļ�ѧ����ʽΪ��_____���������ռ�װ��Ϊ_____������ĸ����
��ʵ������ʯ��ʯ��ϡ���ᷴӦ��ȡ������̼�����г����������Ȼ������壬��ͨ��ʢ�б���̼��������Һ��Fװ������ȥ����������Ӧ��Fװ�õ�_____�˿ڣ���١��ڡ���ͨ�룬F�з����Ļ�ѧ����ʽΪ_____��
��2��Ϊ��̽��������ʣ�������ͼ��ʾ��ʵ�顣

��ͼ����ʾ������һ�������������Һ�ɺ�ɫ��Ϊ����ɫ��֤���������NaOH�������кͷ�Ӧ���ҷ�Ӧ�����Һ��һ��û�е�������_____�������Լ�ʵ��������Һ�����ʳɷֲ�������Ȥ���Է�Ӧ����Һ��Ϊ��ɫ������������ֲ��룺
����1�����ʳɷ�ֻ��NaCl��
����2�����ʳɷ�Ϊ_____��
������ʵ�飩Ϊ����֤�Լ��IJ�����ȷ����������������ʵ�飬�������һ���������ʵ�鱨�棺
ʵ����� | ʵ������ | ʵ����� |
ȡ������ʵ��������Һ���Թ��У������Թ��м���_____ | �۲쵽_____ | ����2��ȷ |
����ͼ�Һͱ���ʾ��ͬʱ����֧����CO2����ͬ�Թֱܷ��ڵ������ˮ��NaOH��Һ�У�һ��ʱ�������Թ���Һ������ҡ�˵��NaOH��CO2�����˷�Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ_____����ʵ�����ҵ�������_____��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com