
分析 (1)根据酒精燃烧,水不燃烧进行解答;
(2)根据甲烷的密度比空气的小解答;
(3)根据爆炸是指可燃物在有限的空间里急剧燃烧,放出大量的热,生成的气体急剧膨胀,发生爆炸;
(4)根据离子符号的意义解答;
(5)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式;
(6)根据物质是由元素组成的,氧化物是由两种元素组成,其中一种含有氧元素的化合物解答.
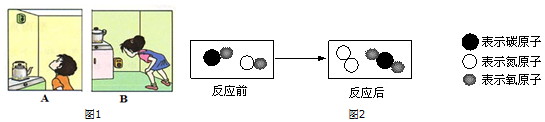
(7)由反应的微观过程图,治理汽车尾气所涉及的反应由2个CO分子与2个NO分子发生反应,生成2个CO2分子和1个N2分子.
(8)久置石灰水的瓶壁上有一层白色固体,是因为氢氧化钙与空气中二氧化碳反应,生成碳酸钙和水,由于碳酸钙是沉淀,必须加酸才能溶解.
(9)根据物质的性质和反应现象分析判断,二氧化碳能使澄清的石灰水变浑浊,二氧化碳不能燃烧,氢气燃烧生成水,一氧化碳燃烧生成二氧化碳.
(10)根据混合气体中含有C、O元素,先计算CO和CO2中C与O元素的质量比,根据混合气体中碳、氧两种元素的质量比为1:2分析其组成.
解答 解:(1)用棉花分别蘸取酒精和水,放在酒精灯火焰上加热片刻,观察到的现象为酒精燃烧,水没有燃烧;通过此实验,可以说明燃烧的条件之一是要可燃物;上述实验中,如果在酒精灯上加热时间较长两个棉球都会燃烧起来,原因是蘸有酒精的棉花球因酒精燃烧放出的热量传给棉花球,使温度达到棉花的着火点,引起棉花燃烧;蘸有水的棉花球当水分蒸发完后,棉花球暴露在酒精灯的火焰中使温度上升达到棉花着火点,且棉花球与空气接触,也达到燃烧所需的三个条件,引起棉花燃烧;
(2)因为天然气的密度比空气小,在家中使用天然气时,天然气泄漏报警器应该安装在上方;
(3)A、一氧化碳属于可燃物,氧气能够支持一氧化碳燃烧,一氧化碳和氧气混合,遇明火可能发生爆炸.
B、氢气属于可燃物,一氧化碳属于可燃物,没有助燃剂,氢气和一氧化碳混合,遇明火不可能发生爆炸.
C、氧气、二氧化碳都不是可燃物,氧气和二氧化碳混合,遇明火不可能发生爆炸.
D、甲烷属于可燃物,氧气能够支持甲烷燃烧,甲烷和氧气混合,遇明火可能发生爆炸.
(4)符号3SO42-中数字“2”的意义是每个硫酸根离子带两个单位的负电荷;
(5)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式2CO2+6H2═4H20+X,反应前碳、氢、氧原子个数分别为2、12、4,反应后的生成物中碳、氢、氧原子个数分别为0、8、4、根据反应前后原子种类、数目不变,则每个X分子由2个碳原子和4个氢原子构成,则物质X的化学式为C2H4.
(6)KClO3中氧元素,不含氧分子,KClO3由三种元素组成,不属于氧化物;
(7)反应后生成生成2个CO2分子和1个N2分子,因此反应中生成的单质和化合物的物质的量之比为1:2;根据反应的化学方程式为:2CO+2NO═N2+2CO2,生成单质与化合物的质量比=28:(44×2)=7:22;
(8)石灰水中的溶质是氢氧化钙,能与空气中的二氧化碳反应生成碳酸钙沉淀和水,该固体的主要成分是CaCO3;由于碳酸钙是一种不溶于水的白色物质,故瓶中常形成一种不溶于水的白色固体;反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O;碳酸钙难溶于水,能与酸反应,实验室洗涤该试剂瓶可用稀盐酸洗去.
(9)混合气体通入澄清的石灰水中,无浑浊现象出现;说明气体中不含二氧化碳.将此气体经尖嘴导管导出后点燃,气体燃烧,在火焰上方罩一个干冷的烧杯,烧杯内壁有水珠出现.说明一定含有氢气,可能含有一氧化碳.
(10)根据混合气体中含有C、O元素,假设气体全为CO,则CO中C、O元素的质量比为12:16=3:4,假设气体全为CO2,则CO2中C、O元素的质量比为12:16×2=3:8,
由混合气体中碳、氧两种元素的质量比为1:2,3:8<1:2<3:4,则混合气体可能为C0、CO2,
又因为氧气中不含碳元素,氧气的存在只能够使C与O元素的质量比的数值变小,
则要满足混合气体中碳、氧两种元素的质量比为1:2,混合气体中必须含有CO,即气体也可能为CO、O2或CO、CO2、O2.
答案:
(1)可燃物;
(2)A;
(3)AD;
(4)每个硫酸根离子带两个单位的负电荷;
(5)C2H4
(6)不含有;不属于;
(7)1:2;7:22;
(8)CO2+Ca(OH)2=CaCO3↓+H2O; C
(9)H2 CO;
(10)DE.
点评 本题主要考查能源和环境方面的知识,化石燃料的使用带来了环境污染,因此积极开发利用新能源,既有利于节约化石燃料,又有利于保护环境.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 敌敌畏由5种元素组成 | |
| B. | 无色、易挥发、易水解等描述的是其化学性质 | |
| C. | 敌敌畏是由4个碳原子、7个氢原子、4个氧原子、2个氯原子和1个磷原子构成 | |
| D. | 敌敌畏是一种较为复杂的氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 本饮料由天然物质配制而成,绝对不含化学物质 | |
| B. | “纯净水”绝对卫生,长期饮用对人体健康有益 | |
| C. | 水是生命之源,我们应该珍惜和爱护水资源 | |
| D. | 矿泉水含有“钾、钙”等对人体有益的成分,这里的“钾、钙”是指它们的单质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | a | b | c | d |
| 反应前质量(g) | 10 | 10 | 10 | 2 |
| 反应后质量(g) | 待测 | 2 | 21 | 2 |
| A. | d一定是该反应的催化剂 | |
| B. | a、b两种物质中元素种类一定与c物质中元素种类相同 | |
| C. | c物质可能是单质 | |
| D. | 反应后a物质的质量为3g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
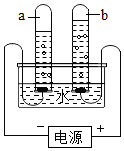 关于电解水实验的叙述正确的是A
关于电解水实验的叙述正确的是A查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com