铁是生活中常用的金属.是某“取暖片”外包装的图片(如图1).该“取暖片”中发热剂主要成分有铁粉、氯化钠、水、活性炭等,其发热是利用铁生锈时会放热的原理.
(1)①发热剂需接触到空气才会发热,原因是铁要与
和
共同作用才会生锈.
②推测发热剂成分中氯化钠的作用是
.
③举例生活中防止金属铁生锈的两种方法:
、
.
(2)化学兴趣小组的甲、乙、丙、丁四位同学对“取暖片”的成分产生了兴趣.
Ⅰ.甲同学预测定“取暖片”中铁粉的含量.取5.7g“取暖片”样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量10.0g)中.在化学反应过程中对烧杯进行了五次称量,数据记录如下表:
| 反应时间 |
t0 |
t1 |
t2 |
t3 |
t4 |
| 烧杯和药品质量/g |
25.7 |
25.6 |
25.5 |
25.5 |
m |
①表格中m的值为
克;反应中共产生氢气
克;
②“取暖片”样品铁粉的质量分数
(精确到0.1%)
③乙同学提出质疑,他认为甲同学的实验测定方案不合理,会导致Fe%结果偏大,试分析可能的原因:
Ⅱ.丙同学预测定一包已变质“取暖片”中Fe
2O
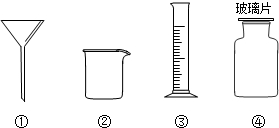
3的质量分数.取10g已变质“取暖片”样品与过量的木炭粉混合,如图2所示装置完成实验.(木炭粉有还原性,NaOH溶液用来吸收反应生成的CO
2,杂质不参加反应)
①实验中持续通入干燥的氮气,加热前缓缓通入一段时间的作用是
②直玻璃管中发生的反应方程式
③充分反应后,丙同学测定NaOH溶液的质量增加了3.3g,通过计算帮助丙同学求出已变质“取暖片”样品中Fe
2O
3的质量分数.
④丁同学提出质疑,他认为丙同学的测定方案不合理,会导致Fe
2O
3%的结果偏小,说一说他的理由:
(1条即可)





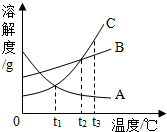 如图中A、B、C分别表示三种物质的溶解度曲线.
如图中A、B、C分别表示三种物质的溶解度曲线. 能源与环境已成为人们关注的热点.
能源与环境已成为人们关注的热点.