
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数。
(1)配制200g质量分数为8%的氢氧化钠溶液。
①计算:需要氢氧化钠固体的质量为 g,水的体积为 mL(水的密度近似看作1g/cm3)。
②称量:调节托盘天平平衡,然后 (按操作的先后顺序选填字母),直至天平平衡。
A.将氢氧化钠固体加入烧杯中 B.按需要添加砝码、移动游码
该步骤中用烧杯而不用纸称量氢氧化钠的原因是 .
③溶解:用量筒量取所需的水,倒入盛有氢氧化钠固体的烧杯里,搅拌,使其溶解,并冷却至室温。
④把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签。
(2)如图表示用上述配制的氢氧化钠溶液与20 g某稀盐酸发生反应后溶液温度的变化情况。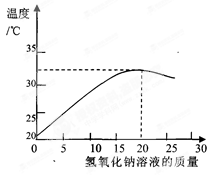
①根据曲线判断,当加入氢氧化钠溶液的质量为 时,反应恰好完全进行。
②当加入15 g氢氧化钠溶液时,所得溶液中的溶质为 (写化学式)。
③试计算上述完全反应后所得溶液的溶质质量分数(请写出计算过程) 。
(1)①16 184 ② B A 氢氧化钠易潮解(或氢氧化钠具有腐蚀性)
(2)①20g ② NaCl、HCl ③ 5.85%
解析试题分析:(1)①根据溶质质量分数计算的表达式可以得出,溶质的质量=溶液的质量×溶质质量分数,需要氢氧化钠固体的质量=200g×8%=16g,水的质量=200g-16g=184g,在根据水的密度1g/cm3,所以水的体积为=184mL;②称量固定物质质量,应先固定砝码和游码,然后再增减药品,所以操作的先后顺序是:B A,由于氢氧化钠易潮解(或氢氧化钠具有腐蚀性),所以称量氢氧化钠固体的时候不能用纸称量,而应该放在玻璃器皿中(烧杯、表面皿)
(2)酸碱中和反应会放出热量,所以随着反应的进行,热量不断放出,当反应停止时,放出的热量最大,图象显示:当加入氢氧化钠溶液的质量为20g,温度最高,表示反应恰好完全进行
(3)因为上题告诉我们:当加入氢氧化钠溶液的质量为20g,表示反应恰好完全进行,所以当加入15 g氢氧化钠溶液时,表示稀盐酸过量,故所得溶液中的溶质除了生成的NaCl,还有过量的HCl
(4)当加入氢氧化钠溶液的质量为20g,质量分数为8%,表示反应恰好完全进行,即消耗的氢氧化钠质量=20g×8%=1.6g,再根据化学方程式:NaOH+HCl=NaCl+H2O,算出生成溶质NaCl的质量
解:设生成溶质NaCl的质量为x
NaOH+HCl=NaCl+H2O
40 58.5
1.6g x
40:58.5 = 1.6g:x
x = 2.34g
∴ 所得溶液的溶质质量分数=2.34g/20g+20g×100%=5.85%[
考点:溶液的配制,中和反应,根据化学方程式进行计算


科目:初中化学 来源: 题型:计算题
我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。小华利用一瓶稀盐酸和相关的仪器,测定黄铜样品的组成(不考虑黄铜中的其他杂质)。将30mL稀盐酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
(1)从上表数据分析,小华用10g合金粉末总共收集到氢气 g;
(2)求该合金中铜的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
进行如图所示的化学实验(装置气密性良好),通过二氧化碳中碳元素与氧元素的质量比来证明二氧化碳的组成,探究过程如下: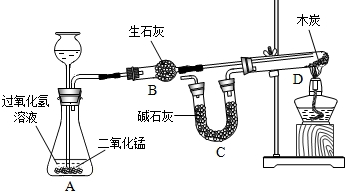
Ⅰ.称量有干燥块状木炭的试管D,质量为a g,装有碱石灰的C装置质量为b g,连接A、B、D装置;
Ⅱ.从长颈漏斗中加入3%的过氧化氢溶液,连接C装置,点燃酒精灯;
Ⅲ.待D中发生反应,熄灭酒精灯,冷却;
Ⅳ.称量试管D及剩余固体质量为cg,装置C的质量为dg;
已知:碱石灰用于吸收二氧化碳,木炭中的杂质不参加反应,B、C中所装药品能完全吸收相关物质.请回答下列问题:
①二氧化锰的作用是 ,装置B的作用是 ,B中发生反应的化学方程式为 ;
②为减少误差,步骤Ⅲ冷却过程中需要注意的问题是 ;
③除②中注意的问题外,该实验过程中还存在一定的误差,你认为产生误差的原因是 ;
④这个实验中如果生成的氧气的质量为16克,则需要参加反应的过氧化氢的物质的量为多少摩尔?(根据化学方程式计算,写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
科学实验提倡绿色环保,对实验装置进行微型化改进是一条很好的途径。图甲是实验室制取并检验CO2的装置,图乙是对图甲实验装置的“微型”化改进后的装置。
(1)图乙中微型塑料滴管在实验中的作用与图甲中的 仪器相同(填字母编号)。
(2)通常用甲装置完成该实验需要的盐酸是“微型”实验装置用量的10倍,采用“微型”实验装置具有的优点是 。
(3)用乙装置完成“制取并检验CO2”的实验,消耗了0.73克10%的盐酸。请计算实验过程中产生CO2的质量是多少克?【(2分);相对原子质量:Ca-40;H-1;C-12;O-16;Cl-35.5】
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
发射通信卫星的火箭用联氨(N2H4)做燃料,用四氧化二氮(N2O4)助燃,生成物不会对大气造成污染。
(1)反应的化学方程式为2N2H4+N2O4=3__________+4H2O,请在横线上填写化学式以完成该化学方程式。
(2)请计算9.6gN2H4完全燃烧需要助燃物N2O4的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
将6.8 g含杂质的锌粒,加入到盛有50.0 g过量的稀硫酸的烧杯中(杂质不溶于水,也不与稀硫酸反应),充分反应后,称得烧杯内物质的总质量为56.6 g。试计算:
(1)生成氢气的质量。 (2)锌粒中所含锌的质量分数(精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
鸡蛋壳的主要成分是磷酸钙.为了测定某鸡蛋壳中碳酸钙的质量分数,小群同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中加入足量的稀盐酸90g,充分反应后,称得反应剩余物为97.14g.(假设其他物质不与盐酸反应)
(1)产生二氧化碳气体 g.
(2)计算该鸡蛋壳中碳酸钙的质量分数.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com