
分析 向硫酸钠和氯化钠组成的混合溶液中加入氯化钡溶液,硫酸钠与氯化钡发生反应生成硫酸钡沉淀和氯化钠,而混合溶液中的氯化钠不与氯化钡反应;至恰好完全反应后,所得溶液为氯化钠溶液,其溶质氯化钠由两部分组成:一部分为原混合物质中的氯化钠,另一部分则是反应生成的氯化钠;
综上所述,原混合物中的硫酸钠的质量,根据反应的化学方程式,可由生成沉淀的质量而求得;所得溶液中溶质质量分数,则是原混合物中氯化钠与生成氯化钠质量总和与所得溶液的质量比.
解答 解:生成硫酸钡的质量:15g+180g+100g-271.7g=23.3g
设硫酸钠质量为x,生成的氯化钠质量为y
Na2SO4+BaCl2=BaSO4↓+2NaCl
142 233 117
x 23.3g y
$\frac{142}{x}$=$\frac{233}{23.3g}$=$\frac{117}{y}$
x=14.2g
y=11.7g
(1)该混合物中硫酸钠的质量分数:$\frac{14.2g}{15g}$×100%=94.7%;
(2)反应后所得滤液中氯化钠的质量为:11.7g+(15g-14.2g)=12.5g
反应后所得滤液中溶质的质量分数:$\frac{12.5g}{271.7g}$×100%=4.6%.
故答案为:(1)该混合物中硫酸钠的质量分数94.7%;
(2)反应后所得滤液中溶质的质量分数4.6%.
点评 利用质量守恒定律,可以很方便地解决反应后所得溶液的问题:反应后溶液质量=固体混合物质量+溶解所加水的质量+加入氯化钡溶液的质量-生成的沉淀质量.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:初中化学 来源: 题型:选择题
| 试剂 | 物质 | 杂质 | 试剂 |
| A | 炭粉 | 铁粉 | 稀盐酸 |
| B | 一氧化碳 | 二氧化碳 | 灼热的氧化铜 |
| C | 氯化钾固体 | 二氧化锰 | 水 |
| D | 氧化铜 | 铜 | 氧气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
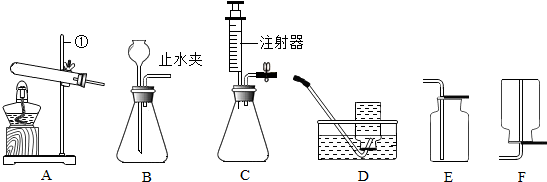
 用推拉注射器活塞的方法可以检查如图装置的气密性.当缓慢推动活塞时,如果装置气密性良好,则能观察到( )
用推拉注射器活塞的方法可以检查如图装置的气密性.当缓慢推动活塞时,如果装置气密性良好,则能观察到( )| A. | 瓶中液面明显上升 | B. | 长颈漏斗内液面上升 | ||
| C. | 瓶内气体分子间的间隔变大 | D. | 长颈漏斗下端管口产生气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 二氧化碳(一氧化碳):通入氧气,点燃 | |
| B. | 硝酸铜溶液(硝酸银):加入足量的铜粉,过滤 | |
| C. | 碳酸钙固体(氯化钙):加入足量的水溶解,过滤、洗涤、干燥 | |
| D. | 氢氧化钠溶液(碳酸钠):加入适量的稀盐酸至不再产生气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 实验序号 | 实验操作 | 实验现象 | 解释及结论 |
| 实验I | 用砂纸擦去镁条表面氧化膜,将其放入盛有适量饱和碳酸氢钠溶液的试管中 | 迅速反应,产生大量气泡和白色不溶物N | / |
| 实验Ⅱ | 将实M气体点燃,并在火焰上方罩一干、冷的小烧杯 | 气体安静燃烧、产生淡蓝色火焰,烧杯内壁有水雾出现 | 气体M是H2,燃烧的化学方程式为 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 钙是人体中的微量元素 | |
| B. | 油脂是重要的营养物质,可大量摄入油脂 | |
| C. | 鸡蛋含有丰富的蛋白质 | |
| D. | 淀粉酶属于糖类,可用于为人体提供能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com