
 SO2;B+D的化学方程式为2Mg+O2
SO2;B+D的化学方程式为2Mg+O2 2MgO;X+D的化学方程式为C+O2
2MgO;X+D的化学方程式为C+O2  CO2;上述化学反应都属于“多变一”的反应特点,为化合反应;
CO2;上述化学反应都属于“多变一”的反应特点,为化合反应;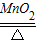 2KCl+3O2↑;2KMnO4
2KCl+3O2↑;2KMnO4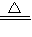 K2MnO4+MnO2+O2↑;2H2O2
K2MnO4+MnO2+O2↑;2H2O2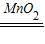 2H2O+O2↑;
2H2O+O2↑; SO2;2Mg+O2
SO2;2Mg+O2 2MgO;C+O2
2MgO;C+O2  CO2;化合反应;
CO2;化合反应;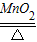 2KCl+3O2↑;2KMnO4
2KCl+3O2↑;2KMnO4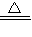 K2MnO4+MnO2+O2↑;2H2O2
K2MnO4+MnO2+O2↑;2H2O2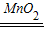 2H2O+O2↑.
2H2O+O2↑.

 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2011届北京市密云县中考一模化学试卷(带解析) 题型:填空题
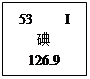
(6分)3月11日,日本东北部地区发生9.0级地震,进而引发福岛第一核电站发生爆炸事故,“I-131” 一下子引起了人们极大的关注。
| | 质子数 | 中子数 | 相对原子质量(近似取整) |
| I-127 | m | 74 | 127 |
| I-131 | 53 | n | 131 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com