
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | |
| 溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | |
分析 (1)食品、药品、营养品、矿泉水等物质中的“钙、镁、钾、钠”等不是以单质、分子、原子等形式存在,而是指元素;
(2)可以根据合理利用水资源和防止环境污染方面进行分析、判断,从而得出正确的结论;
(3)根据活性炭的吸附作用,区分软硬水以及硬水软化的方法进行解答;
(4)根据在化合物中正负化合价代数和为零,结合高铁酸钾(K2FeO4)的化学式进行解答;
(5)根据电解水实验及溶液的有关计算分析解答;
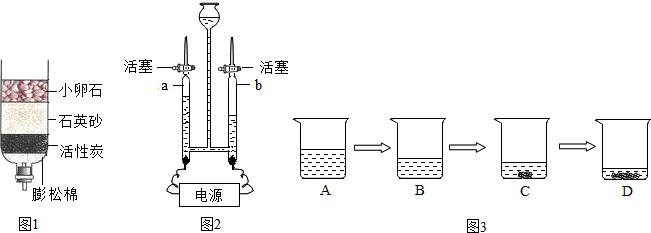
(6)①根据A溶液变化为B溶液,没有晶体析出,BCD都是常温下氯化钠的饱和溶液进行解答;②根据NaCl和KNO3在不同温度时的溶解度变化规律进行分析解答;
解答 解:(1)海水中富含钾、钙、镁等,这里的“钾、钙、镁”指的是元素;
(2)水污染的主要原因有:工业废水、生活废水直接排放,大量使用化肥、农药.所以A、合理使用化肥农药有利于保护水资源,故A正确;B、生活污水直接排放不利于保护水资源,故B错误; C.使用含磷洗衣粉会污染水资源,不利于保护水资源,故C错误;D、工业废水处理达标后排放有利于保护水资源,故D正确;
(3)图1所示装置可以对河水进行简单净化.其中能起到吸附作用的是活性炭;可用肥皂水鉴别净化后的水是硬水还是软水,加入肥皂水振荡,泡沫丰富的是软水,泡沫少的是硬水;若要得到纯度更高的水,实验室中常采用的方法是蒸馏;
(4)解:钾元素显+1价,氧元素显-2价,设铁元素的化合价是x,
根据在化合物中正负化合价代数和为零,
可得:(+1)×2+x+(-2)×4=0,
则x=+6价;
(5)在电解水实验中,生成氢气的体积大,是生成氧气体积的2倍,故b管中产生的气体是氢气;设0.2g硫酸钠溶解在水中,形成的xg溶液中硫酸钠的质量分数为0.8%,则:$\frac{0.2}{x}×100%=0.8%$,解得:x=25(g),(49.8g+0.2)-25g=25g;
(6)①根据A溶液变化为B溶液,没有晶体析出,所以与B溶液中溶质质量相等的溶液是A;BCD都是常温下氯化钠的饱和溶液,所以与B溶液中溶质质量分数相等的溶液是CD;②分析NaCl和KNO3在不同温度时的溶解度可知,W的数值所在的最小范围是36~36.3;因为在这个范围之外,不可能再出现两种物质的溶解度相同的情况.
故答案为:(1)元素;(2)AD;(3)活性炭;肥皂水;蒸馏;(4)+6;(5)氢气;25;(6)A;CD;36~36.3(36<W<36.3).
点评 本题考查元素的概念,水污染的原因,水的净化及软硬水的区别,化合价的计算,溶质质量分数的计算,溶解度的概念等,知识点较多,但基础性较强.


科目:初中化学 来源: 题型:选择题
| A. | 油锅着火用水浇灭 | B. | 电器着火用泡沫灭火器灭火 | ||
| C. | 用明火检查液化气罐是否漏气 | D. | 火场逃生时用湿毛巾捂住口鼻 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
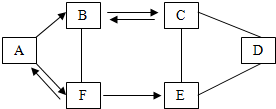 A-F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示.已知A、B、C、D、E是不同类别的物质,C俗称纯碱,E常用作建筑材料,F是人体中含量最多的物质.框图中“-”表示相连的两种物质间能发生化学反应,“→”表示物质间存在转化关系(部分反应物、生成物及反应条件已略去).请回答:
A-F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示.已知A、B、C、D、E是不同类别的物质,C俗称纯碱,E常用作建筑材料,F是人体中含量最多的物质.框图中“-”表示相连的两种物质间能发生化学反应,“→”表示物质间存在转化关系(部分反应物、生成物及反应条件已略去).请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CuO→Cu(OH)2 | B. | CuSO4→Cu | C. | BaSO4→H2SO4 | D. | Fe2O3→FeSO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该反应的微观实质为H+和OH-结合成水分子 | |
| B. | 可用硫酸铜溶液检验反应氢氧化钠是否剩余 | |
| C. | 可用硝酸银溶液检验反应后盐酸是否剩余 | |
| D. | 用pH试纸测得溶液的pH为7时,溶液的离子主要有Na+和Cl- |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氯化钠、硝酸铵、氢氧化钠三种固体 | B. | 氢气、甲烷、一氧化碳三种气体 | ||
| C. | 氯化铵、氢氧化钾、硝酸钠三种溶液 | D. | 酒精、汽油、蒸馏水三种液体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com