解:(1)①最常用的溶剂是水,其化学式为:H
2O.
②金属表面的锈能与酸反应,根据提供的元素硫酸符合要求,其化学式为:H
2SO
4.
③氧气是生命活动中不可缺少的单质,其化学式为:O
2.
④硫是在氧气中燃烧发出蓝紫色火焰的固体,其化学式为:S.
(2)硫和氧气反应生成二氧化硫,反应的化学方程式为:S+O
2
SO
2.
硫酸属于酸、氢氧化钠属于碱,两者反应生成硫酸钠和水,反应的化学方程式为:2NaOH+H
2SO
4═Na
2SO
4+2H
2O.
(3)①葡萄糖的相对分子质量是180,故葡萄糖的摩尔质量是180g/mol.1mol任何物质中含有6.02×10
23个分子,一个葡萄糖分子含有6个氢原子,1mol C
6H
12O
6中含有1mol×6=6mol氢原子.
②该葡萄糖溶液溶质的质量分数为5%的含义是每100份质量的葡萄糖溶液中含有5份质量的葡萄糖.
故答案为:(1)①H
2O;②H
2SO
4;③O
2;④S;(2)S+O
2
SO
2;2NaOH+H
2SO
4═Na
2SO
4+2H
2O;(3)①180g/mol;6;②每100份质量的葡萄糖溶液中含有5份质量的葡萄糖.
分析:(1)首先根据题意确定物质的化学名称,然后根据题目所提供的元素、书写化学式的方法和步骤写出物质的化学式即可.
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
(3)①摩尔质量是指单位物质的量的物质所具有的质量,摩尔质量的单位为g/mol,在数值上等于该物质的相对原子质量或相对分子质量;由葡萄糖分子的构成进行分析计算即可.
②由溶质质量分数的概念进行分析解答.
点评:本题难度不大,掌握化学式与化学方程式的书写方法、化学式的有关计算并能灵活运用是正确解答本题的关键.

 SO2.
SO2. SO2;2NaOH+H2SO4═Na2SO4+2H2O;(3)①180g/mol;6;②每100份质量的葡萄糖溶液中含有5份质量的葡萄糖.
SO2;2NaOH+H2SO4═Na2SO4+2H2O;(3)①180g/mol;6;②每100份质量的葡萄糖溶液中含有5份质量的葡萄糖.

 阅读快车系列答案
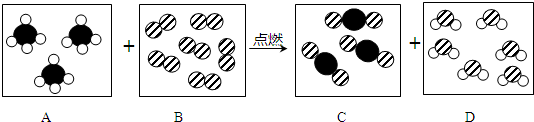
阅读快车系列答案 表示碳原子,
表示碳原子, 表示氧原子,
表示氧原子, 表示氢原子.
表示氢原子.