
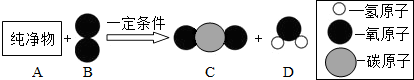
分析 (1)根据质量守恒定律,分析参加反应A物质的质量;
(2)根据质量守恒定律分析A的组成元素及其质量,根据相对分子质量、元素个数比确定化学式,写出反应的哈学方程式.
解答 解:(1)参加反应的A物质的质量是:176g+36g-160g=52g.
(2)根据质量守恒定律及A由两种元素组成可知,A中一定含有碳元素和氢元素.
A含有碳元素的质量为:176g×$\frac{12}{44}$×100%=48g,
A含有氢元素的质量为:36g×$\frac{2}{18}$=4g,
A中碳、氢原子个数比为:$\frac{48g}{12}:\frac{4g}{1}$=1:1;由于相对分子质量为26,故A的化学式为:C2H2.所以反应的化学方程式是:2C2H2+5O2$\frac{\underline{\;一定条件\;}}{\;}$4CO2+2H2O.故答为:(1)44;(2)2C2H2+5O2$\frac{\underline{\;一定条件\;}}{\;}$4CO2+2H2O..
点评 本题考查质量守恒定律的应用,原子个数比等于各元素的质量除以相对原子质量的比.


科目:初中化学 来源: 题型:实验探究题
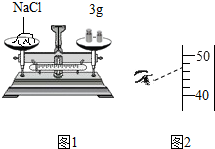 回答下列实验操作的有关问题.
回答下列实验操作的有关问题.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 荔枝的部分营养成分(100克中含) |
| 糖类16.60g 蛋白质0.90g 脂肪0.20g 维生素A 2.00ug 维生素C 41.00ug 钙 2.00mg 鉀 151.00mg 铁 0.40mg 硒 0.14ug… |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 铁、银、铜的金属活动性强弱: | B. | 氮气、氮的化合物与化合价的关系: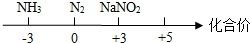 | ||
| C. | 物质溶解度与溶解性的关系: | D. | 物质形成溶液的pH: |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
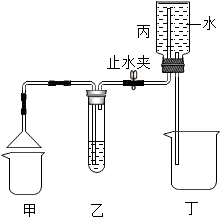 下列是初中常见物质,由下表中元素组成.
下列是初中常见物质,由下表中元素组成.| 元素名称 | 氢 | 碳 | 氧 | 氯 | 钠 | 铁 |
| 元素符号 | H | C | O | Cl | Na | Fe |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 金属镁将成为二十一世纪大有前途的绿色金属材料.
金属镁将成为二十一世纪大有前途的绿色金属材料.| 所加氢氧化钠溶液的次数 | 第一次 | 第二次 | 第三次 |
| 剩余固体的质量/g | 10.6 | 5.2 | 4.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com