
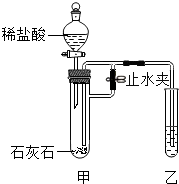
 某化学小组在课外活动时利用如图装置进行实验 (图中铁架台等仪器已略去).
某化学小组在课外活动时利用如图装置进行实验 (图中铁架台等仪器已略去).

科目:初中化学 来源: 题型:
| A、氢氧化钡和稀硫酸 |
| B、锌和稀硫酸 |
| C、氢氧化钠溶液和稀盐酸 |
| D、澄清石灰水和二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:
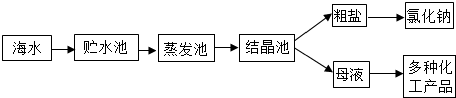
| A、海水进入贮水池,海水的成分基本不变 |
| B、析出晶体后的母液是氯化钠的不饱和溶液 |
| C、在蒸发池中,海水中水的质量逐渐减少 |
| D、在蒸发池中,海水中氯化钠的质量分数逐渐增大 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、石油分馏出汽油、煤油、柴油 |
| B、利用膜法从海水中获得淡水 |
| C、铁矿石冶炼成铁 |
| D、工业上从空气中分离出氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
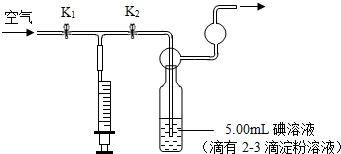
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 抽气次数 | 42 | 38 | 36 | 44 | 40 |
| 二氧化硫的含量 | 是否超标 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com