
���� ��1������ȼ�յ����������ش�
��2�������ڸ���������һ����̼��ԭ����������������ʷ����ش��йص����⣻
��3�����ݷ�Ӧ�Ļ�ѧ����ʽ�����������������������������
��� �⣺��1����ʵ���֪�������Աȣ�˵��ȼ�յ�����֮һ�ǿ�ȼ��ȼ��Ҫ�������Ӵ��������Աȣ�˵��ȼ�յ�����֮һ�ǿ�ȼ��ȼ����Ҫ�¶ȴﵽ�Ż�㣮
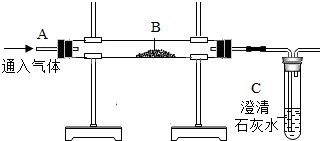
��2��ʵ�����ģ�ҵ��������B��ʢ����������ĩ����A��ͨ��һ����̼һ��ʱ���B���·�����Ƽ��ȣ��ڸ���������һ����̼��ԭ�����������������Ͷ�����̼������B���ɹ۲쵽������Ϊ��ɫ���ʱ�ɺ�ɫ�����ɵĶ�����̼�����������Ʒ�Ӧ������̼��ƺ�ˮ�����ԣ�C��������Ӧ�Ļ�ѧ����ʽΪCa��OH��2+CO2=CaCO3��+H2O��
��3�������ɵ���������x
2Fe2O3�����ڣ�$\frac{\underline{\;ͨ��\;}}{\;}$4Fe+3O2��
320 224
160t x
$\frac{320}{224}=\frac{160t}{x}$ ��ã�x=112t
�ʴ�Ϊ����1����ȼ��ȼ��Ҫ�������Ӵ�����ȼ��ȼ����Ҫ�¶ȴﵽ�Ż�㣻��2����ɫ���ʱ�ɺ�ɫ��Ca��OH��2+CO2=CaCO3��+H2O����3��112�֣�
���� ����ͨ��������װ�ÿ�����ȼ�յ�������������ԭ�����ݻ�ѧ����ʽ�ļ��㣬���ڻ�����֪ʶ���ѶȲ��������е�֪ʶ��ɣ�


 ���ĺ����Ͼ�������ϵ�д�
���ĺ����Ͼ�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | þ���ڿ�����ȼ�շ�������ɫ���棬������������ | |
| B�� | ���ˮ����һ��õ���������ʹ�����ǵ�ľ����ȼ | |
| C�� | ϸ��˿��������ȼ�գ��������䣬���ɺ���ɫ���� | |
| D�� | ��Ũ������Լ�ƿ��ʱ��ƿ���а������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 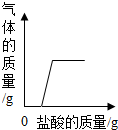 ���ֱ��ʵ�NaOH��Һ�еμ�ϡ���� ���ֱ��ʵ�NaOH��Һ�еμ�ϡ���� | |
| B�� | 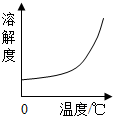 HCl������ܽ�����¶�Ӱ��ı仯���� HCl������ܽ�����¶�Ӱ��ı仯���� | |
| C�� | 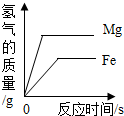 ��������Mg�ۺ�Fe����������ͬŨ�ȵ�ϡ���ᷴӦ ��������Mg�ۺ�Fe����������ͬŨ�ȵ�ϡ���ᷴӦ | |
| D�� | 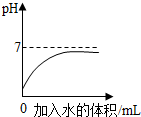 ������Һϡ������pH�ı仯���� ������Һϡ������pH�ı仯���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ż���������ˮ���� | |
| B�� | ������������ʯ�ң��ɸ����������� | |
| C�� | �������ܳ�ȥ�·��ϵ������������黯ԭ�� | |
| D�� | �����ڳ�ʪ�Ļ����б��ڸ���Ļ����и����ױ���ʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 40% | B�� | 44% | C�� | 48% | D�� | 52% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �����������������г��õĴ��ߣ���ͼ��������ʾ��ͼ��
�����������������г��õĴ��ߣ���ͼ��������ʾ��ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
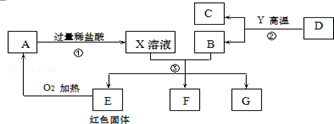
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com