
下图是一盏废旧台灯,某实验小组的同学利用它进行观察分析并完成相关实验。
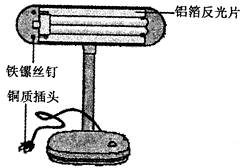
(1)小明发现台灯的铁螺丝钉表面已经锈蚀,原因是铁与空气中的 等发生了化学反应。
(2)小红发现铝箔反光片呈银白色,无锈迹,原因是铝表面有一层致密的氧化膜,生成该氧化膜的化学方程式为 。
(3)铁、铝、铜的金属活动性由强到弱的顺序为 。为了验证三者的金属活动性顺序,小志从实验室领来氯化铝溶液、硫酸铜溶液,并利用台灯提供的一种金属进行实验,即达到了实验目的。实验中发生反应的化学方程式为 。
科目:初中化学 来源: 题型:
生活中处处有化学。请回答以下问题:
(1)薯片等膨化食品等常采用充气包装来保存食品,所充入的气体可能是 。
(2)日常生活中,用铝作为制做炊具的材料是因为 ,铝制的水壶使用后无需用钢丝球擦拭干净,是因为 。
(3)用洗涤剂来去除餐具上油渍,其原理是洗涤剂与油污发生了 作用;洗完后的铁锅用干布抹去其表面的水珠,这样做的目的是 。当关闭燃气阀门后,灶具的火焰也随之熄 灭,其灭火原理是 。
灭,其灭火原理是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
金属镁可用于火箭、飞机、轮船的制造。镁在现代材料工业中需求量逐渐增大。海水中含有约0.129%的镁元素,仅次于氯化钠,总储量约1 800亿吨,开发潜力很大。
(1)在提取镁的生产过程中,需要浓缩海水,提高海水中氯化镁的质量分数,你认为既环保又经济的方法是 ;
(2)浓缩海水中MgCl2的质量分数为9.5%,求要将150吨浓缩海水中MgCl2都转化为Mg(OH)2,理论上需要Ca(OH)2多少吨?
查看答案和解析>>
科目:初中化学 来源: 题型:
铁暴露在空气中会生锈。不知道你注意了没有,将苹果切开不久,果肉上就会产生一层咖啡色的物质的,也好像是生了“锈”一样。某化学活动小组对此进行了探究
【提出问题】切开的苹果“生锈”与什么因素有关?
【猜想与假设】
猜想①:可能与空 气没有关系,只是果肉内物质自身互相反应而“生锈”。
气没有关系,只是果肉内物质自身互相反应而“生锈”。
猜想②:可能是果肉中的物质与空气中氧气作用而“生锈”。
猜想③:可能是果肉中的物质与空气中氮气作用而“生锈”。
猜想④:可能是果肉中的物质与空气中二氧化碳作用而“生锈”。
猜想⑤:可能是果肉中的物质与空气中氧气作用而“生锈”,并且苹果“生锈”的速度还可能与温度有关。
【收集证据】
(一) 查阅资料:已知苹果“ 生锈”是果肉里的物质(酚和酶)与空气中的一种物质发生了反应,生成咖啡色物质。
生锈”是果肉里的物质(酚和酶)与空气中的一种物质发生了反应,生成咖啡色物质。
(二) 实验探究:针对上面的猜想①至猜想⑤,化学活动小组依次设计了实验方案,进行了实验验证,并依次观察到下列实验现象。请你将他们设计的可行的实验探究方案,填写在下表中。
| 猜想 | 可行的实验方案 | 观察到的实验现象 |
| 猜想① | 将一小块果肉浸入蒸馏水中,观察现象 | 果肉表面不变色 |
| 猜想② | 果肉表面变色 | |
| 猜想③ | 果肉表面不变色 | |
| 猜想④ | 果肉表面不变色 | |
| 猜想⑤ | 温度高的先变色 |
【得出结论】 。
【反思与评价】
(1)在②~⑤四种猜想中,你认为猜想 (填代号)最不合理,原因是 。
(2)在验证猜想①时,同学们发现,如果水果与空气隔绝,果肉放在水中时间长了也会变色,其原因是: 。
【应用】根据上述结论,要防止果汁变质,果品加工厂在加工和保存果 汁时可采用的措施是: 。
汁时可采用的措施是: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
早在春秋战国时期,我国就开始生产和使用铁器. 工业上炼铁的原理是利用一氧化碳和氧化铁的反应.某化学兴趣小组利用下图装置进行实验探究,请按要求填空:
工业上炼铁的原理是利用一氧化碳和氧化铁的反应.某化学兴趣小组利用下图装置进行实验探究,请按要求填空:
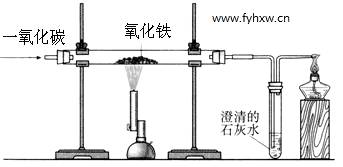
A B C
(1)A中观察到的现象是 。写出CO还原Fe2O3的化学方程式 ;
(2)实验中盛澄清石灰水的试管中可观察到的现象是 ;方程式
(3)右边导气管口放置点燃的酒精灯的目的是
查看答案和解析>>
科目:初中化学 来源: 题型:
全世界每年因生锈损失的钢铁约占世界钢铁年产量的1/4。某学生想探究铁生锈的条件,他将干净的铁钉分别同时放入A、B、C三支试管中进行研究。
(1)请 你帮助该学生完成下列实验设计的内容:
你帮助该学生完成下列实验设计的内容:
| 编号 | 操作方法 | 实验目的 |
| A | 加热烘干试管,小心放入铁钉,塞上塞子 | 探究铁在干燥空气中的生锈情况 |
| B | 放入铁钉,注入蒸馏水浸没铁钉,并用植物油液封 |
|
| C |
| 探究铁在有空气和水时的生锈情况 |
(2)一周后,编号为 的试管中的铁钉最易生锈。
(3)用相同材料制作,经过相同时间防锈处理的铁栏杆,安装在南方比安装在北方更易生锈,其原因是: 。
(4)在焊接铁管时,为了使接口更加牢固,常用稀盐酸清洗接口处的铁锈,该反应的化学方程式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
KNO3和NaCl在不同温度时的溶解度如下表所示。请回答下列问题:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 |
 (1)依据上表数据,绘制KNO3和NaCl的溶解度曲线,右图1中能表示KNO3溶解度曲线的是 (填m或n)。20℃时,KNO3饱和溶液的溶质的质量分数是 (计算结果保留整数)。
(1)依据上表数据,绘制KNO3和NaCl的溶解度曲线,右图1中能表示KNO3溶解度曲线的是 (填m或n)。20℃时,KNO3饱和溶液的溶质的质量分数是 (计算结果保留整数)。
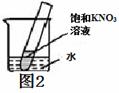 (2)如右图2所示,20℃时,将盛有KNO3饱和溶液的小试管放
(2)如右图2所示,20℃时,将盛有KNO3饱和溶液的小试管放
入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。
加入的物质可能是下列中________(可多选)。
A.氢氧化钠固体 B.生石灰固体
C.冰块 D.硝酸铵固体
(3)今年我区进行了部分学生化学实验操作考试,题目之一是“配制40g质量分数为5%的氯化钠溶液”。该实验的部分操作如下图所示。
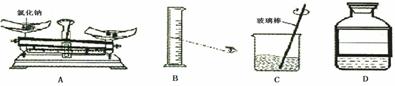
①称量时A出现了右盘低的现象,接下来的操作应该是 (填序号)。
A.左边的平衡螺丝向左调 B.右边的平衡螺丝向右调
C.右盘中减少砝码 D.左盘中增加食盐
②量取水时,如果按照图B方法读数,会使配制的溶液的溶质质量分数 (填“偏大”或“偏小)。
③C中用玻璃棒搅拌的目的 。若配制过程中,转移称量好的氯化钠固体时,有少量洒落在桌子上,其他操作均规范,则所得溶液中氯化钠的质量分数
(填“>”或“<”,或“=”)5%。
④在D中细口瓶所贴的标签上写出合适的内容。
查看答案和解析>>
科目:初中化学 来源: 题型:
人体缺乏维生素C可能得坏血病.维生素C的化学式是C6H8O6,在新鲜的水果、蔬菜中含量都较高.某研究性学习小组测定了某品牌橙汁的维生素C的含量,过程如下:取20.00g橙汁用含碘1.00%的碘溶液与其反应,恰好完全反应时消耗碘溶液25.40g.
试计算:该橙汁中维生素C的质量分数.(计算结果精确到0.01%)(反应的化学方程式C6H8O6+I2=C6H6O6+2HI)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com