
| 化学符号 | 2Fe | ||
| 表示意义 | 三个氧分子 | 一个镁离子 |
分析 原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字.
离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字.
解答 解:由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2Fe可表示为:2个铁原子.
由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,则三个氧分子可表示为:3O2.
由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字,故1个镁离子可表示为:Mg2+.
故答案为:
| 化学符号 | 2Fe | 3O2 | Mg2+ |
| 表示意义 | 2个铁原子 | 三个氧分子 | 一个镁离子 |
点评 本题难度不大,掌握常见化学用语(原子符号、分子符号、离子符号等)的书写方法是正确解答此类题的关键.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
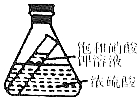 已知浓硫酸(具有强腐蚀性,使用时需注意安全)具有吸水性,可吸收空气中的水蒸气.小明根据这一性质设计了如浓硫酸图所示的趣味实验,一段时间后,小明观察到小试管中有晶体析出.
已知浓硫酸(具有强腐蚀性,使用时需注意安全)具有吸水性,可吸收空气中的水蒸气.小明根据这一性质设计了如浓硫酸图所示的趣味实验,一段时间后,小明观察到小试管中有晶体析出.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 钙的一种特殊氧化物W(CaxOy)广泛应用于水产养殖、污水处理等领域,是优良的供养剂.某化学兴趣小组针对W的组成进行了实验,实验装置如图.
钙的一种特殊氧化物W(CaxOy)广泛应用于水产养殖、污水处理等领域,是优良的供养剂.某化学兴趣小组针对W的组成进行了实验,实验装置如图.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 问题与猜想 | 实验步骤 | 实验现象 | 实验结论 |
| 探究一:固体M是否失效 | 取适量固体M,加入盛有水的烧杯中,用温度计测量加入前后的温度 | 温度没有明显变化 | 固体M失效 |
| 探究二:固体M中是否含有氢氧化钙 | 将上述烧杯内的液体充分搅拌、静置,取上层清液,加入酚酞试液 | 溶液变红 | 有氢氧化钙 |
| 实验步骤 | 现象 | 结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 仪器编号 | 所盛试剂的名称 | 试剂或装置的作用 |
| A | 澄清石灰水 | 证明二氧化碳的存在 |
| B | 浓硫酸 | 吸收水煤气中的水蒸气 |
| C | 因为氢气燃烧生成水,看到烧杯内壁上有水珠出现,能证明H2存在 | |
| D | 一氧化碳燃烧生成二氧化碳,二氧化碳能使澄清石灰水变浑浊能证明CO存在 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com