

分析 (1)根据步骤①将大颗粒粗盐变成了较细粗盐,需要用到研钵进行分析;
(2)根据蒸发过程需要的仪器进行分析;
(3)根据精盐制得率=$\frac{精盐的质量}{粗盐的质量}$×100%分析解答;
A、食盐没有全部溶解即过滤,蒸发后精盐的质量比正常值偏小;
B、蒸发时食盐飞溅剧烈,部分食盐溅出,精盐质量减少;
C、蒸发后,所得精盐很潮湿,造成精盐质量增加;
D、器皿上沾有的精盐没全部转移到称量纸上,精盐质量减少;
(4)根据加入碳酸钠需要在加入氢氧化钡之后,碳酸钠可以除去过量的氢氧化钡,盐酸能除去过量的碳酸钠等知识进行分析;
(5)根据氢氧化钡和硫酸镁反应生成硫酸钡沉淀和氢氧化镁沉淀进行分析;
根据碳酸钠和盐酸反应生成氯化钠、水和二氧化碳进行分析.
解答 解:(1)步骤①将大颗粒粗盐变成了较细粗盐,需要用到研钵,故选:A;
(2)蒸发时用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳、蒸发皿等;
(3)精盐制得率=$\frac{精盐的质量}{粗盐的质量}$×100%
A、食盐没有全部溶解即过滤,造成滤液中食盐的量减少,蒸发后精盐的质量比正常值偏小,则精盐制得率较低,符合题意;
B、蒸发时食盐飞溅剧烈,部分食盐溅出,精盐质量减少,则精盐制得率较低,符合题意;
C、蒸发后,所得精盐很潮湿,含有部分水分,造成精盐质量增加,则精盐制得率较高,不符合题意;
D、器皿上沾有的精盐没全部转移到称量纸上,精盐质量减少,则精盐制得率较低,符合题意;
故选:ABD;
(4)①加入碳酸钠需要在加入氢氧化钡之后,碳酸钠可以除去过量的氢氧化钡,过滤除去沉淀,然后再加入盐酸除去碳酸钠,最后蒸发得到晶体,所以正确的操作顺序是:bdace;
②盐酸和碳酸钠反应会生成二氧化碳,所以步骤c判断加入盐酸“适量”的现象是:不再有气泡产生为止;
(5)①氢氧化钡和硫酸镁反应生成硫酸钡沉淀和氢氧化镁沉淀,化学方程式为:Ba(OH)2+MgSO4=BaSO4↓+Mg(OH)2↓;
②碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑.
故答案为:(1)A;
(2)蒸发皿;
(3)ABD;
(4)①bdace;
②不再有气泡产生为止;
(5)①Ba(OH)2+MgSO4=BaSO4↓+Mg(OH)2↓;
②Na2CO3+2HCl=2NaCl+H2O+CO2↑.
点评 本题综合考查了粗盐提纯实验的有关注意事项,解答时要依据相关知识细心分析.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
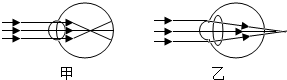 由于不良的学习习惯、上网游戏、偏食等因素的影响,青少年患近视的人数不断增加.请利用所学知识,完成以下与近视相关的部分探究活动.
由于不良的学习习惯、上网游戏、偏食等因素的影响,青少年患近视的人数不断增加.请利用所学知识,完成以下与近视相关的部分探究活动.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 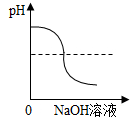 向一定量的稀硫酸中滴加氢氧化钠溶液至过量 | |
| B. |  加热氯酸钾和二氧化锰混合物制氧气 | |
| C. | 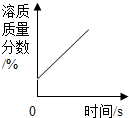 将浓盐酸敞口放置在空气中 | |
| D. | 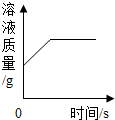 表示向足量的稀HCI中加入少量Fe,溶液质量与时间的关系图 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用水检验NaOH、NH4NO3、CaCO3 | |
| B. | 用燃着的木条检验O2、CH4、CO2 | |
| C. | 用与熟石灰研磨区分CO(NH2)2、NH4Cl、(NH4)2SO4 | |
| D. | 用观察溶液颜色区分CuSO4溶液、Na2SO4溶液、FeSO4溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 选项 | 物质 | 共性 |
| A | 一氧化碳、二氧化碳 | 都有毒性 |
| B | 碳酸钠、氢氧化钠 | 水溶液都呈碱性 |
| C | 浓硫酸、浓盐酸 | 都有挥发性 |
| D | 高锰酸钾、过氧化氢 | 都含有氧元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| OH- | NO3- | SO42- | Cl- | |
| Ni2+ | 不 | 溶 | 溶 | 溶 |
| 金属 | Ni | Zn | Cu |
| 与盐酸反应的现象 | 气体产生缓慢 金属逐渐溶解 | 气体产生激烈 金属迅速溶解 | 无明显现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com