
| A. | 一个分子中含有9个水分子 | |
| B. | 绿原酸在氧气中完全燃烧生成CO2和H2O | |
| C. | 属于氧化物,且氢元素含量最大 | |
| D. | 其中氢、氧元素的质量比为2:1 |
分析 A.根据物质的分子结构来分析;
B.根据物质的组成以及质量守恒定律来分析;
C.根据氧化物的概念以及元素的质量比来分析;
D.根据元素的质量比计算方法来分析.
解答 解:A.分子是由原子构成的,绿原酸分子中不含水分子,故错误;
B.由质量守恒定律,反应前后元素种类不变,绿原酸(C6H18O9)在氧气中,完全燃烧生成CO2和H2O,故正确;
C.氧化物是由两种元素组成的,而绿原酸中含有三种元素,所以绿原酸不属于氧化物,故错误;
D.绿原酸中氢、氧元素的质量比为(1×18):(16×9)=1:8,故错误.
故选B.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
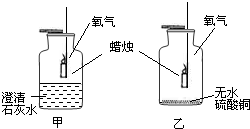 某同学为了研究蜡烛燃烧的产物,设计了以下实验,如图所示.在甲、乙两集气瓶中充满氧气,瓶底分别装有澄清的石灰水和无水硫酸铜白色固体.
某同学为了研究蜡烛燃烧的产物,设计了以下实验,如图所示.在甲、乙两集气瓶中充满氧气,瓶底分别装有澄清的石灰水和无水硫酸铜白色固体.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 农民就地焚烧秸秆 | |
| B. | 深埋含镉、汞的废旧电池 | |
| C. | 工业制酒精C2H4+H2O$\frac{\underline{\;催化剂\;}}{\;}$C2H6O | |
| D. | 化工生产中的废气向高空排放 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 黄白色 黄白色 | B. | 黄白色 蓝色 | C. | 蓝色 蓝色 | D. | 蓝色 黄白色 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
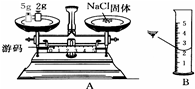 实验室欲配制30g质量分数为25%的NaCl溶液,有下列操作:a.用量筒量取水,b.用天平称取所需氯化钠,c.所需食盐与水混合后搅拌溶解,d.计算所需食盐和水的质量,e.溶液的转存并贴标签.试回答下列问题.
实验室欲配制30g质量分数为25%的NaCl溶液,有下列操作:a.用量筒量取水,b.用天平称取所需氯化钠,c.所需食盐与水混合后搅拌溶解,d.计算所需食盐和水的质量,e.溶液的转存并贴标签.试回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
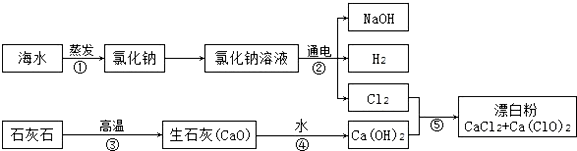
| 实验操作 | 实验现象 | 实验结论 |
| 取少量样品于试管中,滴加足量的稀盐酸. | 有气体产生,气体使石灰水变浑浊. | 猜想2成立 |
| 在上述反应后的试管中加少量品红溶液. | 红色变浅或消失. |
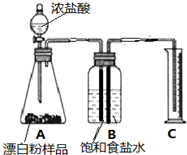
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com