
 元素周期表是我们学习和研究化学的重要工具,它的内容十分丰富.如表是元素周期表部分内容(元素原子结构示意图已给出),请回答下列问题.
元素周期表是我们学习和研究化学的重要工具,它的内容十分丰富.如表是元素周期表部分内容(元素原子结构示意图已给出),请回答下列问题.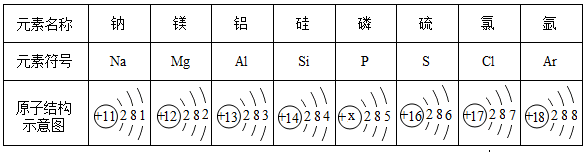 (1)在元素周期表中,原子序数为12的元素符号是Mg,其原子结构示意图如图所示,在化学反应中该原子容易失去(填“得到”或“失去”)电子,形成的离子符号为Mg2+;
(1)在元素周期表中,原子序数为12的元素符号是Mg,其原子结构示意图如图所示,在化学反应中该原子容易失去(填“得到”或“失去”)电子,形成的离子符号为Mg2+;分析 (1)根据元素周期的信息、若最外层电子数≥4,则一般为非金属元素,在化学反应中易得电子,若最外层电子数<4,则一般为金属元素,在化学反应中易失去电子以及元素的分类来分析;
(2)根据原子中,质子数=核外电子数来分析;
(3)最外层具有8个电子的原子具有相对稳定结构.
(4)根据最外层电子数来分析;
(5)总结归纳是学习化学的一种重要方法:元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律.
解答 解:(1)原子序数为12的元素是镁元素,其元素符号为Mg,其原子结构最外层有2个电子,在化学反应中易失去最外层的2个电子,形成带两个单位正电荷的镁离子;故填:Mg;失去;Mg2+;
(2)原子中质子数=核外电子数,则磷原子的核电荷数x=2+8+5=15.由氯原子结构示意图可知,氯原子的最外层有7个电子;故填:15;7;
(3)最外层具有8个电子的原子具有相对稳定结构,表中具有相对稳定结构的元素氩元素.故填:氩;
(4)氯原子的最外层有7个电子,在化学反应中容易得电子形成相对稳定结构;故填:Cl;
(5)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律:从左到右,各元素原子的电子层数相同;从左到右,各元素原子的原子序数依次增加;故填:从左到右,最外层电子数由1到8依次增加.
点评 了解元素周期表的特点及其应用;核外电子在化学反应中的作用;了解原子结构示意图与离子结构示意图的特点.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 工业上可以利用分离液态空气法制氧气 | |
| B. | 氧气能和大多数金属、非金属反应,所以氧气是一种很不稳定的气体 | |
| C. | 氧气在低温、高压的条件下可以转变为液体或固体 | |
| D. | 氧气可使带火星的木条复燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子质量很大,原子质量很小 | |
| B. | 在化学反应中分子可分,原子不能再分 | |
| C. | 原子可以构成分子 | |
| D. | 分子体积大,原子体积小 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验一 | 实验二 | 实验三 | |
| 实验 方案 |  |  | 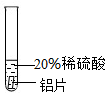 |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色. | 无明显现象 | 铝片表面产生气泡较快. |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | 铝能与稀硫酸发生反应,反应速率较快 |
| 三种金属在金属活动性顺序中的相对位置关系是Al>Cr>Cu | |||
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  向一定量的水中加入生石灰 | B. |  红磷在装有空气的密闭容器中燃烧 | ||
| C. |  向一定质量的烧碱溶液中滴入盐酸 | D. |  向饱和KNO3溶液中加入KMnO4固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com