【答案】
分析:(1)用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,根据化学方程式的书写步骤书写方程式;根据反应物的状态和反应条件选择发生装置:固体加热型和固液常温型;根据气体的密度和溶解性选择收集方法;
(2)实验室通常用稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,写出反应的方程式;制取二氧化碳的药品是石灰石和稀盐酸,属于固体和液体在常温下的发生装置;根据检验二氧化碳使用澄清的石灰水书写方程式;
(3)根据信息提供的反应物的状态和反应条件选择发生装置:固体加热型和固液常温型;根据气体的密度和溶解性选择收集方法;
(4)要得到平稳的氧气流,一定是反应物不能一次加完,要缓缓的添加反应物,使反应持续、匀速的发生.
解答:解:(1)用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,因此反应的化学方程式为:2KMnO
4
K
2MnO
4+MnO
2+O
2↑;
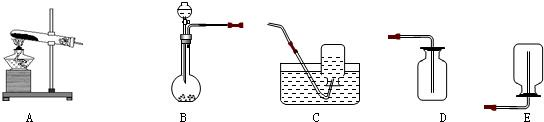
用加热高锰酸钾制取氧气的发生装置属于固体加热型的A装置;用排水法收集的氧气较纯净;
(2)实验室通常用稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的方程式为:CaCO
3+2HCl=CaCl
2+CO
2↑+H
2O;
发生装置的特点属于固液常温型的B装置;检验二氧化碳用石灰水,因为二氧化碳可以使石灰水变浑浊,反应的方程式为:CO
2+Ca(OH)
2=CaCO
3↓+H
2O;
(3)实验室常用加热固体硫酸铵和固体熟石灰的混合物来制取氨气,因此发生装置的特点属于固体加热型的A装置;因为氨气极易溶于水,且密度比空气小,所以只能采用向下排空气法-E装置收集;
(4)①把二氧化锰加入装有过氧化氢溶液的试管中,产生氧气的速度是先快后慢;
②把过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中,反应在持续、匀速的发生,得到的是平稳的氧气流.
故实验现象不相同;
故答案为:(1)2KMnO
4
K
2MnO
4+MnO
2+O
2↑;A;C;
(2)CaCO
3+2HCl=CaCl
2+CO
2↑+H
2O;B;澄清的石灰水;CO
2+Ca(OH)
2=CaCO
3↓+H
2O;
(3)A;E;
(4)否.
点评:(1)本题考查了常见气体的制取装置、收集方法等的选择,并在此基础上进行拓展,关键是明确发生装置、收集方法选择的依据;
(2)考查了分解过氧化氢溶液这一反应,明确单独的过氧化氢溶液在常温下会缓慢的分解生成水和氧气,加入二氧化锰后,过氧化氢分解的速度大大加快.


 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑; K2MnO4+MnO2+O2↑;A;C;
K2MnO4+MnO2+O2↑;A;C;





 写出A、B 两处可观察到的现象,并加以解释:
写出A、B 两处可观察到的现象,并加以解释: