
| A. | 汤姆森 | B. | 卢瑟福 | C. | 波尔 | D. | 牛顿 |
科目:初中化学 来源: 题型:解答题
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有CO2 | 含有CO和CO2 |
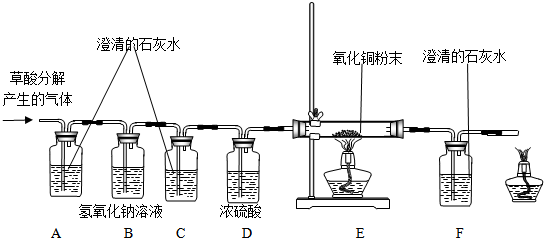
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
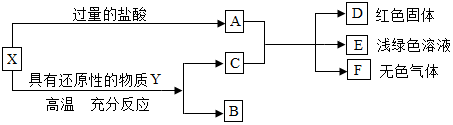
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 第一次 | 第二次 | 第三次 | |
| 所给氧气质量/g | 3 | 6 | 12 |
| 生成二氧化硫质量/g | 6 | 12 | 12 |
| A. | 第一次实验中硫没有燃烧尽 | B. | 只有第二次实验遵守质量守恒定律 | ||
| C. | 三次实验中,气体的质量均增加了 | D. | 第三次实验中氧气没有耗尽 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
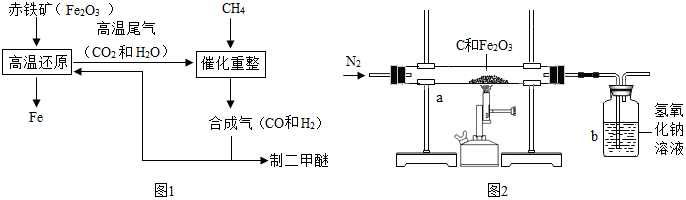
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
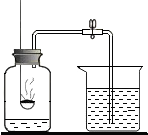 测定空气中氧气含量的实验.
测定空气中氧气含量的实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com