
分析 根据反应前后的质量差即为反应生成二氧化碳的质量,结合二氧化碳的质量可以计算碳酸钠的质量和生成的氯化钠的质量,进一步可以计算纯碱样品中碳酸钠的质量分数.
解答 解:(1)生成二氧化碳的质量为11g+50g-56.6g=4.4g;
故答案为:4.4g.
(2)解:设碳酸钠的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{44}=\frac{x}{4.4g}$
x=10.6g
碳酸钠的质量分数为$\frac{10.6g}{11g}$×100%=96.4%
答:样品中碳酸钠的质量分数为96.4%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
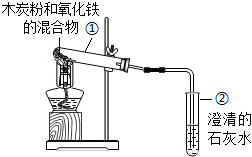
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物 质 | 选用的方法或试剂 | |
| A | 空气和二氧化碳 | 燃着的木条 |
| B | 氧气和二氧化碳 | 通入澄清石灰水 |
| C | 硬水和软水 | 肥皂水 |
| D | 酒精和水 | 看颜色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
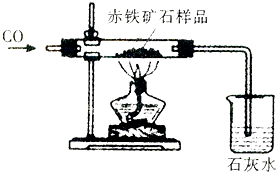
| 反应前 | 反应后 | |
| A组 | 玻璃管和赤铁矿石样品的质量38.5g | 玻璃管和固体物质的质量36.1g |
| B组 | 烧杯和澄清石灰水的质量180.0g | 烧杯和烧杯中物质的质量185.6g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com