
分析 (1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
通常情况下,锌和稀硫酸反应生成硫酸锌和氢气,氢气难溶于水,密度比空气小;
(2)注射器能够控制液体药品的流量,从而能够控制反应速率;
(3)根据气体的性质可以判断收集气体的方法;
(4)根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置.
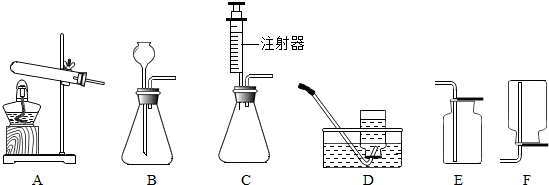
解答 解:(1)用B装置制取氧气时,因为不需要加热,应该是利用过氧化氢制取氧气,反应的化学方程式是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
B装置还可以用来制取二氧化碳或氢气,该反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑或Zn+H2SO4═ZnSO4+H2↑.
故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;二氧化碳或氢气;CaCO3+2HCl═CaCl2+H2O+CO2↑或Zn+H2SO4═ZnSO4+H2↑.
(2)若选C做气体发生装置,其优点是能够控制反应速率.
故填:能够控制反应速率.
(3)一氧化氮在空气中能与氧气迅速反应生成红棕色的二氧化氮气体,因此不能用排空气法收集,一氧化氮不溶于水,可以用排水法收集,即用D装置收集.
故填:D.
(4)实验室选择气体发生装置时,应考虑反应物状态和反应条件,选择气体收集装置时,应考虑气体的密度、溶解性、能否和空气中的物质反应等.
故填:反应物状态;反应条件;气体的密度、溶解性、能否和空气中的物质反应等.
点评 本题主要考查反应表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | 干煸芸豆 | B. | 牛奶 | C. | 肉末鸡蛋 | D. | 稀饭 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com