
【题目】M元素的单质是当今世界高科技领域发展较快,用途较广的有色材料,如可做火箭头、导弹点火头、航天器元部件及照明弹等,其原子结构示意图如图
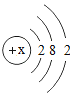
(1)M元素的名称是_____,位于周期表中第_____周期。
(2)M元素的化学性质与下列_____(填字母)元素的化学性质相似。
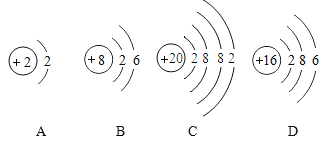
(3)M元素的离子符号是_____。
(4)M元素与地壳中含量最多的非金属元素形成化合物的化学式_____。
【答案】镁 3 C Mg2+ MgO
【解析】
(1)当质子数=核外电子数,为原子,x=2+8+2=12,其核内质子数为12,为镁元素;
周期数=原子核外电子层数,M元素的原子核外有3个电子层,则在元素周期表中,该元素位于第3周期;
(2)元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,M元素的最外层电子数为2,C中最外层电子数也为2,最外层电子数相同,化学性质最相似;A中原子的最外层电子数为2,但其核外只有一个电子层,属于稀有气体元素的原子,化学性质稳定;尽管最外层电子数相同,但它们化学性质不相似;
(3)M原子的核内质子数为12,为镁原子;M原子的最外层电子数为2,在化学反应中易失去2个电子而形成带2个单位正电荷的阳离子,其离子符号为Mg2+;
(4)M元素为镁元素,与地壳中含量最多的非金属元素为氧元素,镁元素显+2价,氧元素显﹣2价,形成的化合物为:MgO。


科目:初中化学 来源: 题型:
【题目】如图是实验室制取CO2及进行性质实验的部分装置。
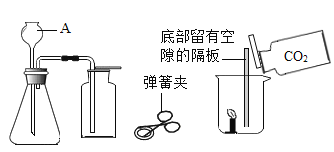
(1)CaCO3固体与稀盐酸反应生成CO2气体的化学方程式是________。
(2)加入药品。添加块状CaCO3固体时,为避免打破锥形瓶,应将锥形瓶______,再放入固体。添加盐酸时,将稀盐酸从_____(填仪器A的名称)倒入锥形瓶至_____。
(3)如图所示,向放置有燃着的蜡烛的烧杯中倒入CO2,观察到的现象是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某探究学习小组欲利用下列装置进行相关实验制取的探究。
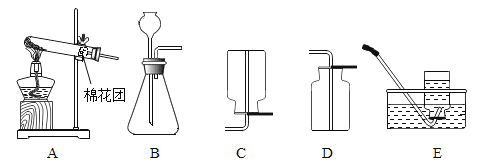
(1)利用上图A、E装置的组合可以制取某种气体,写出实验室制取该气体的化学方程式_。
(2)实验室通常用上图中装置B与____(选填字母)的组合制取二氧化碳。为了得到纯净、干燥的二氧化碳气体,如图除杂装置的导管按气流方向连接的顺序正确是____(选填字母)。
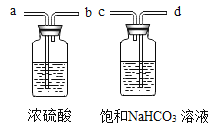
A a→b→d→c B b→a→c→d
C d→c→a→b D c→d→b→a
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过学习,你已经掌握了实验室制取气体的有关知识。请结合如图回答。
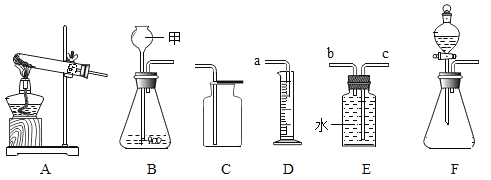
(1)仪器甲的名称是__________。
(2)实验室选B装置作为实验室制取氧气的发生装置,反应的化学方程式为:__________,某同学用C装置收集氧气,验满方法是_______________。
(3)实验室可用B或F装置制二氧化碳,选用F相对于B装置的主要优点是___________________________。
(4)某同学用D、E装置收集一定量的氢气,装置接口连接的顺序为_____(填接口字母),量筒的作用是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定一瓶标签已被部分腐蚀的过氧化氢溶液的溶质质量分数(过氧化氢占溶液的含量),小明开展了如下探究:
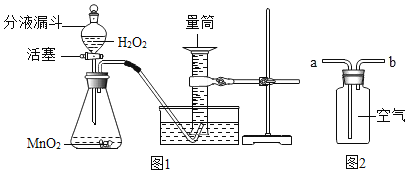
Ⅰ.连接仪器,检查装置气密性。
Ⅱ.取适量的二氧化锰粉末放入锥形瓶中,用托盘天平称取一定质量的过氧化氢(H2O2)溶液,倒入分液漏斗中。
Ⅲ.如图1所示安装好实验装置。
Ⅳ.打开分液漏斗活塞,制取并测量产生氧气的体积。根据该温度时氧气的密度计算出氧气质量(量筒足够大,能够收集产生的氧气)。
Ⅴ.根据氧气的质量,利用过氧化氢与氧气之间的质量比例关系求出过氧化氢质量;用过氧化氢的质量除以称量的过氧化氢溶液质量得出过氧化氢溶液溶质质量分数。
Ⅵ.回收锥形瓶中的二氧化锰,洗净仪器放回原处。
回答下列问题:
(1)该反应的表达式为__。
(2)该实验中,不考虑反应温度对实验的影响,冷却后读数,收集氧气的体积__产生的氧气体积(填“大于”、“小于”或“等于”)。
(3)读取氧气的体积时,如果仰视读数,则测量结果__(填“大于”、“小于”或“等于”)实际值。
(4)若用如图2收集氧气,氧气应该从__(“a”或“b”)通入。
(5)二氧化锰在该实验中的作用是__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳及其化合物在生活和生产中有着广泛的用途。请回答下列问题:
(1)列车利用碳滑板与接触网接触来获取电。碳滑板通常用石墨制成,是因为石墨具有润滑作用和__性。
(2)农场利用实验室制二氧化碳的原理给大棚中的蔬菜“施肥”,写出制取CO2的化学反应方程式______。
(3)为提高能源利用率,某科研团队发明了一氧化碳燃料电池,成功地将化学能直接转化为______能,并将该过程生成的CO2用 KOH 吸收,实现“碳的零排放”,写出该反应的化学方程式____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以大豆等为原料可制成豆制品。豆制品的营养主要体现在蛋白质含量上,还含有钙、磷、铁等矿物质以及维生素B1、B2等;此外,所含豆固醇与不饱和脂肪酸有较好的祛脂作用,且热量很低。2种豆制品的制作过程如下:
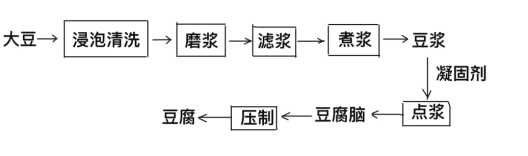
[豆腐的制作]
[腐乳的制作]
豆腐切块→长出毛霉→加盐腌制(析出水分,豆腐块变硬,抑制微生物生长,避免豆腐块腐败变质)→加卤汤装瓶(形成独特风味)→密封腌制发酵。前酵是培菌累积酶系的过程,一般为36~48h, 后醇是酶系作用于腐乳坯体的过程,耗时较长,一 般为3~6个月。腐乳发酵过程中食盐和嘌呤含量较高,高血压、心血管病、痛风、肾病患者及消化道溃疡患者,宜少吃或不吃。腐乳发醇过程中食盐含量对组分的影响如图所示。
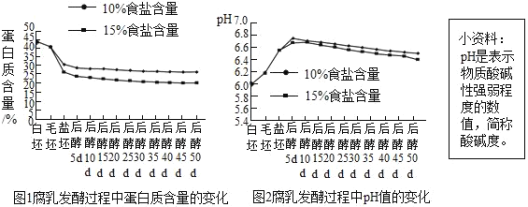
回答问题:
(1)制作豆腐工艺中,磨浆过程属于_______变化。豆制品中含有人体所需要的营养素主要有___ 、 无机盐和维生素。
(2)腐乳制作过程中不应加入过多食盐,理由是______。
(3)腐乳发酵过程中,后酵5d后,酸性会逐渐____(填“增强”、“减小”或“不变”)。
(4)肥胖和心血管病患者可适当多吃一些豆制品的理由是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的锌粉,参加反应的锌的质量与溶液中金属离子种类的关系(如图所示)。下列说法不正确的是()
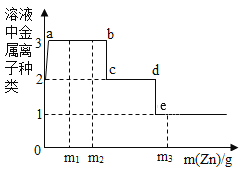
A.a~b间(不含两点)的溶液中金属离子为Zn2+、Ag+、Cu2+
B.c~d间(不含两点)的溶液中金属离子为Zn+、Cu2+
C.当参加反应的锌的质量为m3时,溶液中金属离子为Zn+
D.当参加反应的锌的质量分别为m1、m2时,溶液中Cu(NO3)2的质量分数相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二甲醚可以代替氟利昂作制冷剂,对臭氧层没有破坏作用,工业制备二甲醚(CH3OCH3)的化学方程式为![]() ,下列有关说法正确的是( )
,下列有关说法正确的是( )
A.该反应为化合反应
B.X的化学式为CO2
C.二甲醚碳元素的质量分数为26%
D.二甲醚中碳、氢、氧元素的质量比为2:6:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com