
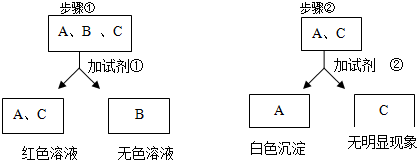
分析 根据氢氧化钠和氢氧化钙都是碱,都显碱性,会使酚酞变红色,盐酸显酸性不会使酚酞变红色,氢氧化钠和氢氧化钙中阳离子不同,可以加入碳酸钠等,在氢氧化钙中会生成白色沉淀,在氢氧化钠中没有现象,所以加入的试剂①是酚酞,试剂②是碳酸钠,A是氢氧化钙,B是盐酸,C是氢氧化钠;根据推出的反应物、生成物书写方程式.
解答 解:(1)氢氧化钠和氢氧化钙都是碱,都显碱性,会使酚酞变红色,盐酸显酸性不会使酚酞变色,氢氧化钠和氢氧化钙中阳离子不同,可以加入碳酸钠等,在氢氧化钙中会生成白色沉淀,在氢氧化钠中没有现象,所以加入的试剂①是酚酞,试剂②是碳酸钠;
故答案是:①酚酞;②碳酸钠溶液;
(2)氢氧化钙和试剂碳酸钠溶液发生反应生成白色的碳酸钙沉淀和氢氧化钠;
故答案是:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)A和B的反应是氢氧化钙和盐酸反应生成氯化钙和水,其反应化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O;
故答案是:Ca(OH)2+2HCl=CaCl2+2H2O.
点评 本题考查了常见物质的鉴别,在解此类题时,首先分析需要鉴别的物质的性质,然后选择适当的试剂,出现不同的现象即可鉴别.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
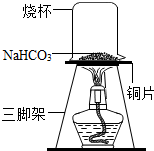
| 序号 | 实验操作 | 预期现象 | 结论 |
① | 取少量加热后的固体产物放入试管A中,加入适量蒸馏水,充分振荡溶解,滴加足量氯化钙溶液,振荡,静置. | 产生白色沉淀 | 产物含碳酸钠 |
| ② | 取操作①后的上层清液于试管B中,滴加酚酞试液. | 酚酞试液不变色 | 产物不含NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
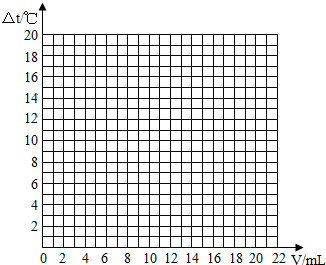
| 加入盐酸的体积(V)/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 溶液温度变化(△t)/℃ | △t1 | 5.2 | 9.6 | 12.0 | 16.0 | 18.2 | 16.7 | 15.7 | 14.7 | 13.7 | 12.9 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
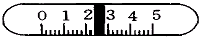 用托盘天平称量烧杯和药品,当天平达到平衡时游码的位置如图所示:
用托盘天平称量烧杯和药品,当天平达到平衡时游码的位置如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com