
| 物质名称 | 乙烷 | 丙烷 | 丁烷 | 戊烷 | 己烷 |
| 沸点 (℃) | -88.6 | -42.2 | -0.5 | 36.1 | 69.2 |
| A. | 乙烷、丙烷和丁烷 | B. | 乙烷、丙烷 | C. | 只有乙烷 | D. | 戊烷和己烷 |
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:选择题
| A. | 运用活性炭净水能够降低水的硬度 | |
| B. | 适量补钙有利于青少年身体发育 | |
| C. | 滥用食品添加剂有害人体健康 | |
| D. | 回收塑料既节约资源又减少“白色污染” |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
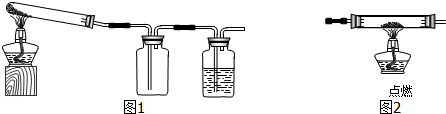
| 装置 | 反应前 | 反应后 |
| A | 试管的质量36.2 克 氧化铜和炭粉混合物的质量20.0克 | 试管和固体物质的质量54.8 克 |
| B | 反应后瓶内液体比反应前增重1.1 克 | |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
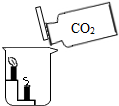 如图所示,将二氧化碳倒入烧杯中.现象:底层蜡烛先熄灭,上层蜡烛后熄灭;
如图所示,将二氧化碳倒入烧杯中.现象:底层蜡烛先熄灭,上层蜡烛后熄灭;查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
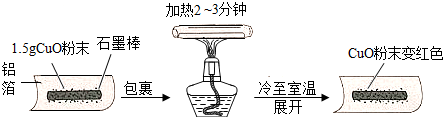
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
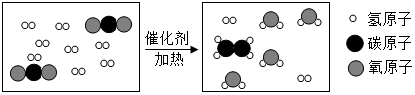 探究是一种重要的学习方式,是充分理解学科本质的基本途径.图是用过氧化氢溶液制取氧气后所做的两个实验.
探究是一种重要的学习方式,是充分理解学科本质的基本途径.图是用过氧化氢溶液制取氧气后所做的两个实验.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
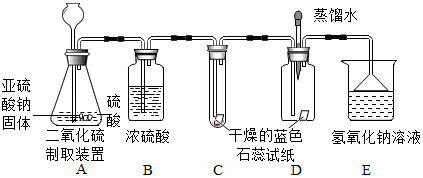
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 往试管中倾倒液体药品时,标签要向着手心 | |
| B. | 称量时砝码放在托盘天平左盘中 | |
| C. | 可以向燃着的酒精灯中添加酒精 | |
| D. | 取用固体药品只能用药匙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com