
【题目】元素周期表是化学学习的重要工具,依据下表回答问题:
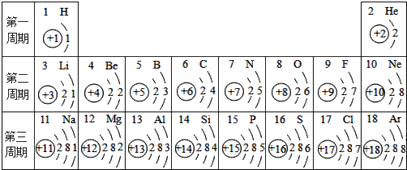
(1)表中16号元素属于______(填“金属”或“非金属”)元素,在化学反应中比较容易_____(填“失去”或“得到”)电子,形成_____(填离子符号),该元素的化学性质与表中______元素相似。
(2)由11号元素与17号元素组成的常见物质的名称是______。
(3)根据上表中原子核外电子排布规律,原子序数为20元素的原子结构示意图为______,该元素的原子在化学反应中容易形成离子,该离子符号是______.
(4)表中同一周期原子的核外电子排布规律是_______________________。
【答案】非金属 得到 S2- 氧 氯化钠 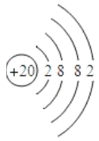 Ca2+ 由左至右,原子的最外层电子数依次增1
Ca2+ 由左至右,原子的最外层电子数依次增1
【解析】
(1)由图可知,16号元素为硫元素,该元素名称带有石字旁,属于非金属元素,故填非金属;
由硫原子结构示意图可知,硫原子的最外层电子数为6,在化学反应中易得到电子,故填得到;
一个硫原子在化学反应中能得到2个电子,形成带2个单位负电荷的硫离子,根据离子符号的写法:在相应元素符号的右上角先写出所带电荷的数目,再写出电荷的电性,则硫离子的符号为S2-,故填S2-;
硫原子与表中氧原子的最外层电子数都为6,所以硫元素与氧元素的化学性质相似,故填氧。
(2)11号元素为钠元素,17号元素为氯元素,这两种元素组成的化合物的名称是氯化钠,故填氯化钠。
(3)依照表中原子核外电子排布规律,原子序数为20元素的原子核外有4个电子层,第一层有2个电子,第二层有8个电子,第三层有8个电子,第四层有2个电子,所以该元素原子的结构示意图为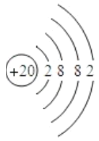 ;
;
20号元素为钙元素,钙原子的最外层电子数为2,在化学反应中易失去这两个电子,形成带2个单位正电荷的钙离子,根据离子符号的写法:在相应元素符号的右上角先写出所带电荷的数目,再写出电荷的电性,则钙离子的符号为Ca2+,故填Ca2+。
(4)同一周期原子就是元素周期表中同一横行中的元素原子,由图可知,表中同一周期原子的核外电子排布规律是由左至右,原子的最外层电子数依次增1,故填由左至右,原子的最外层电子数依次增1。


科目:初中化学 来源: 题型:
【题目】化学学习中常常需要控制变量、设计对比实验对物质进行探究.
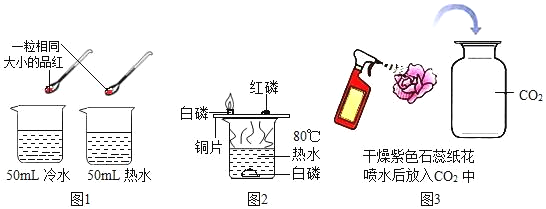
(1)图1所示实验中,两杯水都变红,但热水变红的时间比冷水要短.由此说明_____.
(2)如图所示实验中,观察到_____现象,可知可燃物燃烧的条件是:需要温度达到可燃物的着火点和_____.
(3)图3所示实验观察到的现象是_____,为探究CO2能跟水反应,还应补充的实验是_____.CO2与水反应的化学方程式为_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属材料在生产生活中十分广泛
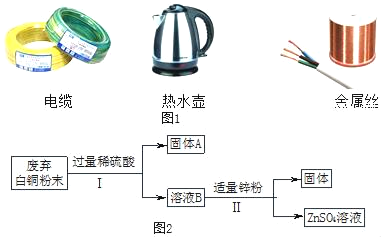
(1)根据图1金属应用实例推断,金属具有的物理性质有_____(答两点)
(2)生铁和钢都是铁的合金,二者性能不同的原因是_____;
(3)写出工业上以赤铁矿为原料炼铁过程中,一氧化碳与氧化铁发生反应的化学方程式_____;每年因腐蚀而消费掉的金属材料数量惊人,铁生锈的条件是_____。
(4)某课外小组用废弃白铜(Cu、Ni)粉末分离得到Cu、Ni两种金属,其主要流程如图2(部分反应产物在图中已略去):已知:Ni与Fe化学性质相似,常见化合价为+2价。
①中反应的化学方程式是_____。
②由上述流程得出Cu、Ni、Zn的金属活动性由强到弱的顺序是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组在探究碱的化学性质时,做了如图所示的两个实验。
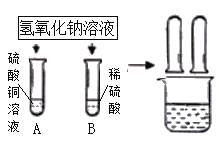
(1)写出A试管中发生反应的化学方程式________。
(2)实验结束后,同学们将A、B两试管中的废液倒入同一洁净的烧杯,烧杯中出现蓝色沉淀.小组同学将烧杯中的物质进行了过滤,对滤液中成分有如下猜想:
(提出猜想)甲:滤液中的溶质是Na2SO4
乙:滤液中的溶质是Na2SO4 、 H2SO4
丙:滤液中的溶质是Na2SO4 、 CuSO4
丁:滤液中的溶质是______
(交流讨论)同学们对以上的猜想提出质疑,认为猜想______不合理,理由是______
(设计实验)同学们通过以下的实验对猜想进行验证,请你完成实验报告。
实验内容 | 预计现象 | 预计结论 |
①取少量滤液于试管中,观察 | 溶液呈无色 | 猜想_____不成立 |
②继续在上述试管中加入______ | ______ | 猜想丁成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钠是一种重要的化工原料.电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应为:2NaCl+2H2O![]() Cl2↑+H2↑+2NaOH,现取一定质量的质量分数为10%的NaCl溶液进行电解,当氯化钠完全反应时,停止通电,生成氯气的质量与时间的关系如图所示.请计算:
Cl2↑+H2↑+2NaOH,现取一定质量的质量分数为10%的NaCl溶液进行电解,当氯化钠完全反应时,停止通电,生成氯气的质量与时间的关系如图所示.请计算:
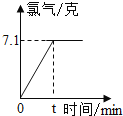
(1)参加反应的氯化钠是多少克______?生成氢气多少______?
(2)完全反应后所得溶液中溶质的质量分数是多少______?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室污染成为环境保护的关注点。某学校排放的废水中含有碳酸钠,未经处理,会造成污染,化学兴趣小组的同学对废水处理设计了如图所示的实验方案。

试计算:
(1)反应生成CO2气体的质量是多少g。
(2)反应后所得溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时,现象如图2,甲、乙两种物质的溶解度曲线如图3,请结合图示回答下列问题
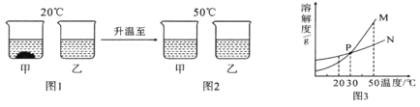
(1)图1中一定为饱和溶液的是__________________。
(2)图2中甲、乙两溶液中溶质质量分数的大小关系为______________。
(3)图3中表示乙的溶解度曲线是______,P点表示的含义是__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】资源、能源与环境已成为人们日益关注的问题。
材料:可燃冰外观像冰,在地球上的储量大约是已探明其他化石燃料总量的2倍;同等条件下,可燃冰燃烧产生的能量比传统的化石燃料要多出数十倍,而且燃烧后不产生任何残渣和废气,是公认的地球上尚未开发的储量丰富的新型能源。
(1)目前,人类使用的化石燃料主要包括煤、石油、_______。
(2)为减少污染、提高煤的利用率,可在高温条件下将其转化为可燃性气体,此过程的微观示意图如下,该反应的化学方程式是___________。
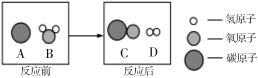
(3)为方便贮存和运输,天然气通常被压缩到容积较小的钢瓶中,而可燃冰却很难被压缩。试从分子的角度分析,其中的原因是_________________。
(4)可燃冰作为新型能源,相比传统化石燃料具有很多优点,主要是_____(填序号)。
A 储量丰富 B 燃烧值大 C 清洁、无污染 D 易于开采
(5)用干燥、纯净的一氧化碳还原氧化铁的实验装置如图:
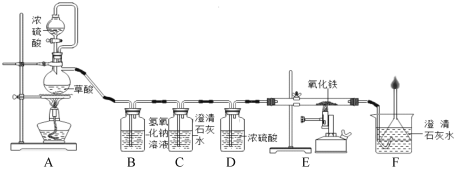
A装置是实验室里用草酸(H2C2O4)和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:H2C2O4  H2O+CO2↑+CO↑。请回答下列问题:
H2O+CO2↑+CO↑。请回答下列问题:
①C装置无明显现象,C装置的作用是_____________。
D装置中浓硫酸的作用是______________。
②E装置中反应的化学方程式是________________。
③F装置的作用是___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】NOS加速系统可以使车辆引擎在瞬间爆发出强大的动力,从而极大的提高行驶速度。
资料:在同温同压下,气体的体积之比等于分子个数之比。
(1)原理是将N2O通入发动机在高温的条件下分解生成N2和O2,写出该反应的化学方程式______。
(2)开启NOS加速系统可以使燃料得更充分燃烧,原因是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com