
分析 (1)根据浓盐酸和浓硫酸的性质进行分析解答;
(2)可以根据稀硫酸的质量分数越小,酸性越强,质量分数越大,酸性越弱的特点进行综合分析、判断,酸溶液的pH小于7,酸性越强,pH越小;
(3)盐酸、硫酸都能与金属氧化物反应;通常制作氯化锌用盐酸;除杂不得引入新的杂质.
解答 解:
(1)盐酸的溶质是氯化氢具有挥发性,氯化氢会与水蒸气生成盐酸小液滴,而硫酸的溶质是硫酸,不具有挥发性,打开盛浓盐酸和浓硫酸试剂瓶的瓶盖,立即就能把它们区分开来的原因是:瓶口出现白雾的是浓盐酸,因为浓盐酸有挥发性;
(2)硫酸的质量分数越大,pH越小,10%的稀硫酸溶质质量分数大于2%的稀硫酸,故10%的稀硫酸的酸性强于2%的稀硫酸,其pH小,故填:小于;
(3)
①盐酸、硫酸都能与金属氧化物反应,都能用于金属表面除锈;
②实验室不用硫酸制取二氧化碳,因为硫酸与碳酸钙反应生成的硫酸钙微溶,包在大理石的表面,阻碍反应的进行;
③除杂不得引入新的杂质,而硫酸与氢氧化钠反应会生成新的杂质硫酸钠;
答案:
(1)瓶口出现白雾的是浓盐酸,因为浓盐酸有挥发性;
(2)小于;
(3)②③;
点评 本题主要考查了溶液的质量分数大小与溶液pH大小的关系问题,完成此题,可以依据已有的知识结合酸的性质进行.


 53随堂测系列答案
53随堂测系列答案科目:初中化学 来源: 题型:选择题
| A. | 向NaOH溶液中通入CO2 | B. | 向CaO中滴加蒸馏水 | ||
| C. | 向Fe2(SO4)3溶液中滴加NaOH溶液 | D. | 向BaCO3中滴加稀HNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
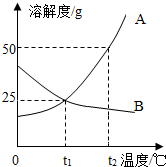 如图为A、B两种固体物质的溶解度曲线,下列说法不正确的是( )
如图为A、B两种固体物质的溶解度曲线,下列说法不正确的是( )| A. | t1℃时,100gA、B的饱和溶液所含的溶质质量相等 | |
| B. | t2℃A、B的饱和溶液降温到t1℃时,溶质质量分数都减小 | |
| C. | t2℃时,75gA的饱和溶液中加50g水得到20%的溶液 | |
| D. | B的溶解度随温度升高而减小 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
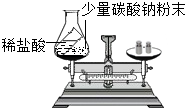 为验证质量守恒定律,某同学设计了如图实验.请回答:
为验证质量守恒定律,某同学设计了如图实验.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 鉴别NaOH和NaCl固体 | 分别加少量水溶液 |
| B | 鉴别棉线和羊毛线 | 点燃后闻气味 |
| C | 除去H2中少量的水蒸气 | 将混合气体通过装有浓硫酸的洗气瓶 |
| D | 检验Na2CO3溶液中是否混有NaCl | 加入过量的稀盐酸后,再滴加硝酸银溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com